
科目: 来源: 题型:解答题
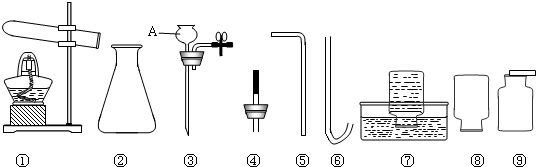
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
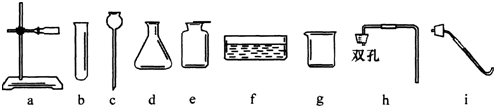
查看答案和解析>>
科目: 来源: 题型:单选题
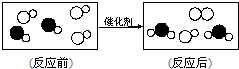 如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的园球代表不同原子.下列说法错误的是
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的园球代表不同原子.下列说法错误的是查看答案和解析>>
科目: 来源: 题型:填空题
| 名称 | 乙醇 | ②________ | 甲烷 | 碳酸氢钠 |
| 俗名 | ①________ | 生石灰 | 沼气 | ④________ |
| 化学式 | C2H50H | CaO | ③________ | NaHCO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
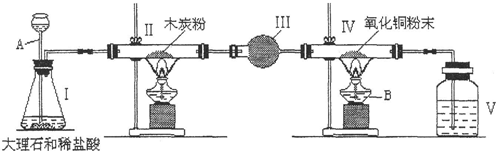
| 反虑前 | 反应后 | |
| 硬质玻管+样品的质量 | 40.0g | 38.4g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com