
【题目】下图为太平洋不同海域沿岸洋流分布示意图。完成下列问题。
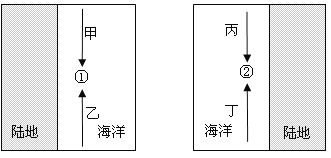
【1】
A. 甲洋流增温增湿 B. 乙洋流是暖流
C. 丙洋流增温增湿 D. 丁洋流是暖流
【2】
A. ①处沿岸是亚热带常绿硬叶林带 B. ②处沿岸是温带落叶阔叶林带
C. ①处的渔场是北海道渔场 D. ②处的渔场是北海渔场
【答案】
【1】B
【2】C
【解析】试题分析:
【1】下图中洋流分布在大陆西岸,根据世界洋流分布规律(如下图所示)可知,该区域交汇处应该位于赤道附近,大陆东岸高纬度地区的洋流无法交汇,那么丙、丁都是从较高纬度流向赤道属于寒流,故排除选项C、D;左图中洋流分布在大陆东岸,而且两洋流相汇,应分布在北半球的中高纬度地区,而且甲是寒流,降温减湿,乙是暖流, 故选项B正确。
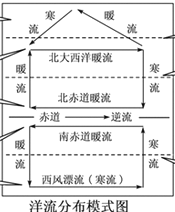 【2】结合上题分析,①处位于中纬度大陆东岸,沿岸应该是温带落叶阔叶林带,故排除选项A;②处位于赤道附近,沿岸是热带雨林带,故排除选项B;由于②处在赤道附近,结合世界主要渔场分布可知该地没有世界性大渔场,故排除选项D;①处若位于亚欧大陆东岸,应该是北海道渔场,故选项C正确。
【2】结合上题分析,①处位于中纬度大陆东岸,沿岸应该是温带落叶阔叶林带,故排除选项A;②处位于赤道附近,沿岸是热带雨林带,故排除选项B;由于②处在赤道附近,结合世界主要渔场分布可知该地没有世界性大渔场,故排除选项D;①处若位于亚欧大陆东岸,应该是北海道渔场,故选项C正确。


 阅读快车系列答案
阅读快车系列答案科目:高中地理 来源: 题型:
【题目】厄立特里亚国家以雨育农业(只靠天然降水而无任何人工灌溉的农业)为主,80%的人口从事农牧业。该国生产落后,丰年粮食自给率仅60%~70%。读图回答下列问题。
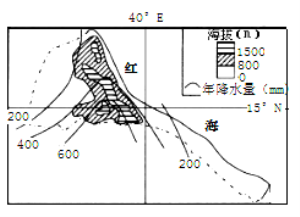
【1】该国农业生产的主要特点是
A.小农经营 B.商品率高
C.机械化水平高 D.灌溉技术先进
【2】目前,该国提高粮食单产的最有效措施是
A.扩大耕地面积 B.改善土壤肥力
C.完善水利设施 D.覆膜种植农作物
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】John was late for the business meeting because his flight had been___by a heavy storm
A.kept
B.stopped
C.slowed
D.delayed
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】落户湖北省黄石市黄石港区江北工业园的中国-东盟北斗科技城(左图),计划建成面向全球、特别是以泰国、马来西亚等国家为主的东盟地区,集北斗应用和服务产业体系、北斗产业孵化体系、科技体验和休闲观光体系、国际高端学术交流和技术外包服务体系等为一体的科技城(右图)。据此完成下列各题。
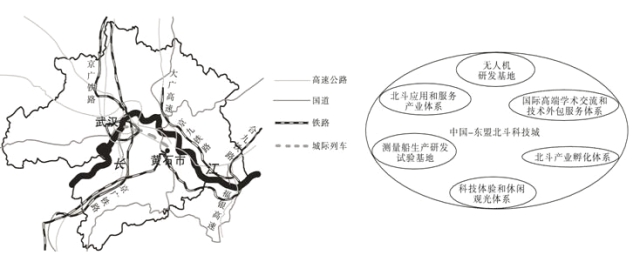
【1】测量船研发基地和无人机研发基地进入该科技城有利于
A.共同利用公共服务 B.及时把握研发动态
C.共同处理废弃物质 D.开拓产品销售市场
【2】中国-东盟北斗科技城的建设,有利于湖北省
A.提高城市化水平 B.开发能源矿产资源
C.缩小城乡间差异 D.促进产业结构升级
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】氢能是一种极具发展潜力的清洁能源,以太阳能为热能,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
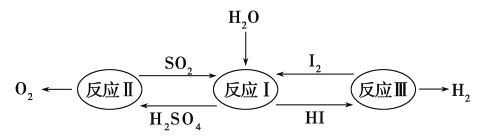
(1)反应Ⅰ的化学方程式是________________。
(2)反应Ⅰ得到的产物用I2进行分离。该产物的溶液在过量I2的存在下会分成两层——含低浓度I2的H2SO4层和含高浓度I2的HI层。
①根据上述事实,下列说法正确的是________(选填序号)。
a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
②辨别两层溶液的方法是____________________。
③经检测,H2SO4层中c(H+)∶c(SO![]() )=2.06∶1,其比值大于2的原因______________________。
)=2.06∶1,其比值大于2的原因______________________。
(3)反应Ⅱ:
2H2SO4(l)===2SO2(g)+O2+2H2O(g)
ΔH=+550 kJ·mol-1
它由两步反应组成:
ⅰ.H2SO4(l)===SO3(g)+H2O(g)
ΔH=+177 kJ·mol-1
ⅱSO3(g)分解。
L(L1,L2),X可分别代表压强或温度,下图表示L一定时,ⅱ中SO3(g)的平衡转化率随X的变化关系。
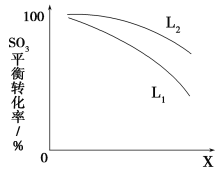
①X代表的物理量是________。
②判断L1,L2的大小关系,并简述理由:________________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】有资料认为NO、NO2不能与Na2O2反应。某小组学生提出质疑,从理论上分析Na2O2和NO2都有氧化性,根据化合价升降原则提出假设并进行探究:假设Ⅰ.Na2O2能氧化NO2
假设Ⅱ.NO2能氧化Na2O2
(1) 小组甲同学设计了如图实验装置,并进行如下实验:
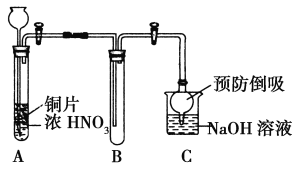
① 试管A中发生反应的化学方程式是______________________________。
② 待试管B中收集满气体,向试管B中加入适量Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带余烬的木条迅速伸进试管内,看见木条复燃。甲同学认为假设Ⅱ正确;乙同学认为该装置不能达到实验目的,为达到实验目的,在A、B之间增加一个装置,该装置的作用是___________________。
③ 乙同学用改进后装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;但带余烬的木条未复燃。得出结论:假设Ⅰ正确。NO2和Na2O2反应的方程式是_____________________________。
(2) 丙同学认为NO易被O2氧化,更易被Na2O2氧化。
查阅资料:①2NO+Na2O2===2NaNO2
② 6NaNO2+3H2SO4===3Na2SO4+2HNO3+4NO↑+2H2O
③ 酸性条件下,NO或NO![]() 都能与MnO
都能与MnO![]() 反应生成NO
反应生成NO![]() 和Mn2+
和Mn2+
丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。

① A装置中盛装Cu片的仪器名称是_____________________,B中观察到的主要现象是______________________,F装置的作用是______________________________。
② 在反应前,打开弹簧夹,通入一段时间N2,目的是______________________________。
③ 充分反应后,检验D装置中产物是NaNO2还是NaNO3的实验方法是_______________ _____________________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】A、B、C、D均为短周期元素。A、B可形成两种液态化合物甲和乙,其最简式分别为BA和B2A。A与D可形成气态化合物DA、DA2。B与D可形成一种极易溶于水的碱性气体X。B与C可形成极易溶于水的酸性气体Y。Y溶于水能完全电离。已知X分子与乙分子中的电子数相等,Y分子与甲分子中的电子数相等。请回答:
(1)甲的电子式为___________。
(2)常温下,aL pH为2的Y溶液与bL pH为12的氢氧化钠溶液混合后,所得溶液pH=3,则a:b=___________。
(3)X溶于水后发生电离,写出电离方程式____________,已知X在液态时和水一样,可发生微弱的电离,产生两种含相同电子数的粒子。请写出它的电离方程式:___________。
(4)X与甲在一定条件下可发生反应,生成无污染的产物,写出反应的化学方程式_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com