
【题目】关于氢键的下列说法正确的是( )
A.由于氢键的作用,使NH3、H2O、HF的沸点反常,且沸点高低顺序为HF>H2O>NH3
B.氢键只能存在于分子间,不能存在于分子内
C.没有氢键,就没有生命
D.相同量的水在气态、液态和固态时均有氢键,且氢键的数目依次增多
 名校课堂系列答案
名校课堂系列答案科目:高中地理 来源: 题型:
【题目】Who ________ that played a trick on the new English teacher?
A.it was
B.was it
C.he was
D.was him
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】---- What about my idea?
---- Very good! But not many people ________ the idea that money brings happiness.
A. subscribe to
B. take to
C. contribute to
D. relate to
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】阅读图文材料,完成下列要求。
太平洋中某岛国经济发展较快,与许多国家有着长期友好的贸易关系。该国农业主产甘蔗、椰子、香蕉等经济作物,其中蔗糖出口占总出口的70%。A港口位于该国某主岛的东南沿海,是该国的最大海港,是南太平洋的航运中心,有南太平洋的“十字路口”之称。国家一半以上的人口分布在该主岛上。下图示意该国主岛及A、B两地气候资料。
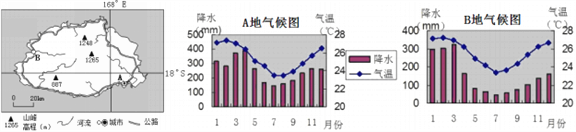
(1)指出A地比B地种植甘蔗更有利的气候条件并简述原因_________。
(2)说明该国发展甘蔗制糖业的有利条件_______。
(3)该岛居民建议进一步扩大甘蔗的种植,对此你是否赞同?试说明理由_____。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】位于南极洲麦克默多湾(约78°S)以西的麦克默多干燥谷,大约有200多万年没有降水,是地球上条件最严酷的荒漠,也是南极大陆唯一没有冰雪覆盖的地方。干燥谷中有冰层达数米厚的盐湖。下图为南极洲麦克默多干燥谷景观图。据此完成下列问题。

【1】麦克默多干燥谷降水少的原因是
A. 受极地东风的影响,风力强劲 B. 受高压控制,盛行下沉气流
C. 受寒流影响,降温减湿 D. 受地形影响,地势高
【2】麦克默多干燥谷全年平均气温为-30℃,而冰层下的湖水水温却高达25℃,比较温暖,其主要原因是
A. 湖底地壳活跃,释放大量热能
B. 夏季冰川融水注入,增加了湖水的温度
C. 阳光透过冰层,冰层阻止其热量散失
D. 纬度高终年寒冷,湖水温度变化小
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】【2017桃城区校级模拟】化学上常用AG表示溶液中的lg![]() .25℃时,用0.100molL﹣1的NaOH溶液滴定20.00mL 0.100molL﹣1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
.25℃时,用0.100molL﹣1的NaOH溶液滴定20.00mL 0.100molL﹣1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
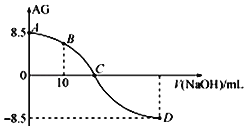
A.D点溶液的pH=11.25
B.B点溶液中存在 c(H+ )﹣c(OH﹣ )=c(NO2﹣ )﹣c(HNO2)
C.C点时,加入NaOH溶液的体积为20 mL
D.25℃时,HNO2的电离常数Ka=1.0×10﹣55
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】Please remind me______he said he was going.I may be in time to see him off.
A.where
B.when
C.how
D.what
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】【2017湖南三模】常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA﹣,Ⅲ代表A2﹣),根据图示判断,下列说法正确的是( )
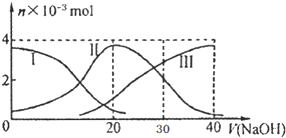
A.H2A在水中的电离方程式是:H2A═H++HA﹣;HA﹣H++A2﹣
B.当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序为:c(Na+)>c(HA﹣)>c(H+)>c(A2﹣)>c(OH﹣)
C.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水中大
D.当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+c(HA﹣)+2c(H2A)═c(A2﹣)+2c(OH﹣)
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】【2017硚口区校级模拟】已知:常温下浓度为0.1molL﹣1的下列溶液的pH如表:下列有关说法正确的是( )
溶质 | NaF | × | Na2CO3 |
pH | 7.5 | 9.7 | 11.6 |
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF
B.若将CO2 通入0.1 molL﹣1Na2CO3溶液中至溶液中性,则溶液中2 c (CO32ˉ)+c (HCO3ˉ)=0.1 molL﹣1
C.根据上表,水解方程式ClOˉ+H2OHClO+OHˉ的平衡常数K≈10ˉ7.6
D.向上述NaClO溶液中通HF气体至恰好完全反应时:c(Na+)>c(Fˉ)>c(H+)>c(HClO)>c(OHˉ)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com