
【题目】下列分散系最不稳定的是
A.向CuSO4溶液中加入NaOH溶液得到的分散系
B.向水中加入食盐得到的分散系
C.向沸水中滴入FeCl3饱和溶液得到的红褐色液体
D.向NaOH溶液中通入CO2得到的无色液体
 名校课堂系列答案
名校课堂系列答案科目:高中地理 来源: 题型:
【题目】中国和印度既是两个发展中的大国,又是两个人口大国。读以下图表,回答下列问题。
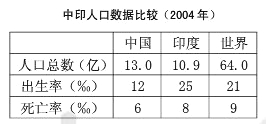
(1)根据表中数据计算,中、印两国中2004年新增人口较多的是_______,中国和印度两国新增人口占世界的_____%。
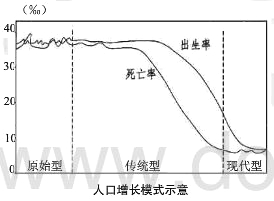
(2)若将世界人口增长模式划分为原始型、传统型和现代型三种类型,根据中、印两国的人口出生率和死亡率判断,目前中国的人口增长模式属于________型,印度的人口增长模式属于________型。
(3)中印两国每年净增人口数量大,其共同原因是_____________________________。从中、印两国人口年龄结构看,中国突出的人口问题是________________,其带来的社会问题是________________________________________________。与中国相比,印度人口增长压力更大的原因是________________________________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】读某盛行风向形成示意图,完成下列问题.

【1】该风盛行的主要季节,下列现象不可能出现的是( )
A.天山雪线上升 B.长江口海水盐度较大
C.地球向近日点移动 D.北极极昼范围在扩大
【2】导致图中风向发生改变的主要动力是( )
A.摩擦力 B.风力 C.地转偏向力 D.水平气压梯度力
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】读“某海区洋流分布示意图”和“某海域等温线分布图”,回答下列问题。
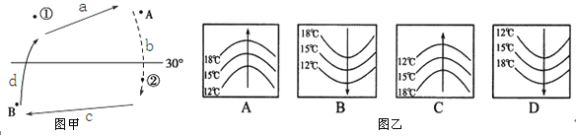
(1)图甲表示的海域位于 半球中低为度海区。
(2)图乙中能正确表示图甲中b洋流的是 (填图中字母代号)。
(3)图甲d洋流对沿岸气候的影响是 。
(4)若该环流位于太平洋,图中①处附近海域为世界著名的 渔场,其形成的主要原因是 。
(5)若②海区有一大型油轮发生石油泄漏,洋流对消除海洋污染的有利方面是 ,不利方面是 。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】在铁制品上镀上一层锌层,以下电镀方案中合理的是( )
A.锌作阳极,铁制品作阴极,溶液中含Fe2+
B.锌作阴极,铁制品作阳极,溶液中含Zn2+
C.锌作阴极,铁制品作阳极,溶液中含Fe3+
D.锌作阳极,铁制品作阴极,溶液中含Zn2+
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】298 K时,在20.0 mL 0.10 mol![]() 氨水中滴入0.10 mol
氨水中滴入0.10 mol![]() 的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol
的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol![]() 氨水的电离度为1.32%,下列有关叙述正确的是
氨水的电离度为1.32%,下列有关叙述正确的是
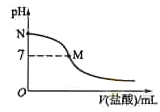
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0 mL
C.M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D.N点处的溶液中pH<12
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】Syrian state media says a bomb has exploded at the state talevision building in Damascus(大马士革),___several people
A.wounding
B.having wounded
C.to wound
D.to have wounded
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】10 ℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50 ℃ |
pH | 8.3 | 8.4 | 8.5 | 8.8 |
甲同学认为:该溶液pH升高的原因是HCO![]() 的水解程度增大,碱性增强。
的水解程度增大,碱性增强。
乙同学认为:该溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度________NaHCO3的水解程度(填“大于”或“小于”)。
丙同学认为甲、乙的判断都不充分。
丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则________(填“甲”或“乙”)的判断正确。试剂X是________。
A.Ba(OH)2溶液 B.BaCl2溶液
C.NaOH溶液 D.澄清石灰水
(2)将加热煮沸后的溶液冷却到10 ℃,若溶液的pH________8.3(填“高于”、“低于”或“等于”),则________(填“甲”或“乙”)判断正确。
(3)查阅资料,发现NaHCO3的分解温度为150 ℃,丙断言________(填“甲”或“乙”)判断是错误的,理由是______________________。
(4)关于NaHCO3饱和水溶液的表述正确的是_______________________。
a.c(Na+)=c(HCO![]() )+c(CO
)+c(CO![]() )+c(H2CO3)
)+c(H2CO3)
b.c(Na+)+c(H+)=c(HCO![]() )+c(CO
)+c(CO![]() )+c(OH-)
)+c(OH-)
c.HCO![]() 的电离程度大于HCO
的电离程度大于HCO![]() 的水解程度
的水解程度
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是一种重要的化工产品,易溶于水,遇酸易分解,Na2S2O3稀溶液与BaCl2溶液混合无沉淀生成。工业制备Na2S2O3的反应为: S(s)+Na2SO3(aq)![]() Na2S2O3(aq),产品中常含有少量Na2CO3 、 Na2SO3和Na2SO4。实验室拟用如下实验装置在C中制备Na2S2O3。
Na2S2O3(aq),产品中常含有少量Na2CO3 、 Na2SO3和Na2SO4。实验室拟用如下实验装置在C中制备Na2S2O3。

请回答下列问题:
(1)按如图所示装置进行实验,装置A中反应的化学方程式是______________________。装置C中可观察到溶液先变浑浊,后又澄清,生成的浑浊物质化学式为___________。
(2)装置B的作用为_________;为保证Na2S2O3的产量,实验中通入的SO2不能过量,原因是_________。
(3)为了验证固体硫代硫酸钠工业产品中含有碳酸钠,选用下列装置进行实验:
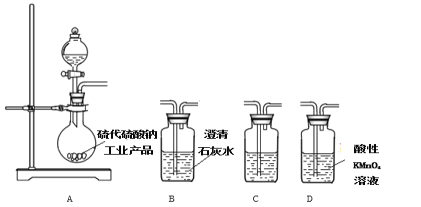
①实验装置的连接顺序依次________________(填装置的字母代号),装置C中的试剂为____________。
②能证明固体中含有碳酸钠的实验现象是__________________。
(4)若要检验固体硫代硫酸钠工业产品中含有Na2SO3,需先加水配成稀溶液,再依次加入的试剂为_____________________和品红溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com