
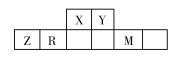
【题目】有五种短周期主族元素,它们在周期表中的位置如图所示,已知R元素的最高正化合价与最低负化合价的代数和为0。
完成下列问题:
(1)Z元素在周期表中的位置是__________________,同周期原子半径最大的元素是____________(填元素符号)。
(2)X的简单氢化物与M的单质,在一定条件下可以发生置换反应,化学方程式为______________,还原产物中含有的化学键类型有____________。
(3)我国发射“神舟”系列飞船的长征火箭,常以X、Y的液态氢化物做燃料。已知X、Y的两种氢化物电子数相等,并且反应时生成两种无毒、无污染的物质。
①写出两种氢化物反应的化学方程式______________________________,反应中氧化剂和还原剂的物质的量之比为____________。
②X的液态氢化物的电子式__________________。
(4)下列说法能证明R、Y非金属性强弱的是____________。
A.R和Y的单质在一定条件下能生成RY2
B.Y单质常温下是气体,R单质是固体
C.Y的氢化物稳定性大于R的氢化物
D.自然界中存在Y单质不存在R单质
【答案】(13分)
(1)第三周期、第IIIA族(2分) Na(1分)
(2)8NH3+3Cl2![]() N2+6NH4Cl(2分) 离子键、共价键(2分)
N2+6NH4Cl(2分) 离子键、共价键(2分)
(3)①N2H4+2H2O2![]() N2+4H2O(1分) 2∶1(2分) ②
N2+4H2O(1分) 2∶1(2分) ②![]() (1分)
(1分)
(4)AC(2分)
【解析】根据元素在周期表中关系,可知R位于第三周期,最高正化合价与最低负化合价的代数和为0,则R只能为Si,Z为Al,X为N,Y为O,M为Cl。
(1)铝在周期表中的位置是第三周期、第IIIA族;第三周期原子半径最大的元素是Na。
(2)NH3与Cl2发生置换反应:8NH3+3Cl2![]() N2+6NH4Cl;在反应中NH4Cl是还原产物,属于离子化合物,含有共价键和离子键。
N2+6NH4Cl;在反应中NH4Cl是还原产物,属于离子化合物,含有共价键和离子键。
(3)①N、O形成的等电子液态氢化物分别为:N2H4和H2O2,二者反应的化学方程式为:N2H4+2H2O2![]() N2+4H2O;在反应中H2O2为氧化剂,N2H4为还原剂,物质的量之比为2∶1。②N2H4的电子式为:
N2+4H2O;在反应中H2O2为氧化剂,N2H4为还原剂,物质的量之比为2∶1。②N2H4的电子式为:![]() 。
。
(4)根据Si与O2的反应生成SiO2,由于O的非金属性大于Si,所以O显负价,A项正确;根据单质的状态不同不能判断Si和O的非金属性强弱,B项错误;气态氢化物越稳定说明对应元素非金属性越强,C项正确;Si在自然界中不存在单质,O则存在氧气,但不能说明二者非金属性强弱,D项错误。


科目:高中地理 来源: 题型:
【题目】下列有关显微镜使用的相关叙述中,正确的是 ( )
A.目镜放大倍数与镜身长短成正比,而物镜的放大倍数与镜身长短成反比
B.在不调换物镜的情况下也能准确判断视野中异物所在位置
C.物镜放大倍数越小,镜头越长,观察时,物镜与标本的距离越短
D.用高倍镜观察标本时,要使物像更清晰,需调节粗准焦螺旋
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】下图中的a图为“某大陆局部地域自然带分布现状示意图”,b图为该地域“未来可能出现的自然带分布示意图”。回答下列问题。
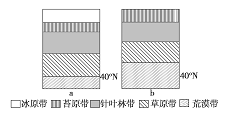
【1】导致图示变化过程的原因,还可能会造成:
A.自然灾害减少 B.全球各纬度粮食增产
C.雪线高度下降 D.北半球农耕区的北界纬度提高
【2】造成图示变化过程的人类活动可能是:
A.积极兴修水利工程 B.植树造林,保护环境
C.大量燃烧矿物燃料 D.开发新能源,提倡清洁生产
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】下面是有机合成的三个步骤:①对不同的合成路线进行优选;②由目标分子逆推原料分子并设计合成路线;③观察目标分子的结构,正确的顺序为( )
A.①②③ B.③②① C.②③① D.②①③
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】自20世纪60年代,甲国开始在邻近乙国边境的地区设立边境工业区,吸引乙国的企业来此投资建厂,并从乙国进口原料和零部件,加工、组装成品后再销往乙国。目前,这些边境工业区已发展成规模不等的工业中心(见下图)。据此回答下列各题。
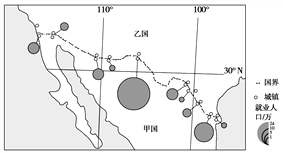
【1】据图文资料推断,与乙国相比,甲国
A. 劳动力价格较低 B. 技术水平较高
C. 消费市场较广 D. 资金较雄厚
【2】影响甲国边境工业区区位选择的主导因素是
A. 廉价劳动力 B. 交通运输
C. 研发能力 D. 环境质量
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】—Don’t make a joke of his height.He is very___
A.active
B.creative
C.conservative
D.sensitive
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】在0.1 mol·L1 CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO+H+,对于该平衡,下列叙述正确的是
CH3COO+H+,对于该平衡,下列叙述正确的是
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1 mol·L1 HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com