
| A. | 某溶液中滴加KSCN溶液呈无色,再滴加氯水后出现血红色,该溶液中含有Fe2+ | |
| B. | 某溶液中滴加NaOH溶液后再滴加CaCl2溶液出现白色沉淀,该溶液中含有CO32- | |
| C. | 某溶液中滴加氨水后再滴加NaOH溶液出现白色沉淀,该溶液中含有Al3+ | |
| D. | 某溶液中滴加足量稀盐酸后,再滴加BaCl2溶液才出现白色沉淀,该溶液中含有SO42- |
分析 A、亚铁离子被氯气氧化为铁离子,滴加KSCN溶液会出现红色;
B、溶液中的HCO3-滴入氢氧化钠反应生成碳酸根离子结合钙离子生成沉淀;
C、溶液中铝离子和氨水反应生成氢氧化铝白色沉淀,加入氢氧化钠沉淀溶解;
D、溶液中加入足量稀盐酸无现象,再加入氯化钡溶液出现白色沉淀证明含有硫酸根离子.
解答 解:A、某溶液中滴加KSCN溶液呈无色,一定不含铁离子亚铁离子,再滴加氯水,亚铁离子被氯气氧化为铁离子,溶液会出现红色,溶液中含有Fe2+,故A正确;
B、溶液中的HCO3-滴入氢氧化钠反应生成碳酸根离子结合钙离子生成沉淀,所以原溶液中不一定含有碳酸根离子,故B错误;
C、溶液中铝离子和氨水反应生成氢氧化铝白色沉淀,加入氢氧化钠溶液沉淀会溶解,证明无铝离子,故C错误;
D、溶液中加入足量稀盐酸无现象,再加入氯化钡溶液出现白色沉淀证明含有硫酸根离子,是硫酸根离子的检验方法,故D正确;
故选AD.
点评 本题考查了离子检验的实验方法和干扰离子的区分,掌握离子性质是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤ | B. | ①②③⑤ | C. | ③④⑤ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量为16g的O2和O3的混合气体中所含的氧原子的个数为NA | |
| B. | 18 g NH4+含有质子数为10NA | |
| C. | 1 mol过氧化钠与足量水反应时,转移电子的数目为2NA | |
| D. | 0.1 mol•L-1的NaCl溶液中,Na+与Cl-的离子总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①②③ | B. | 只有①② | C. | 只有②③ | D. | 只有①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4HCO3 | B. | KCl | C. | CO(NH2)2 | D. | KNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
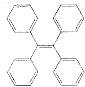 有机物TPE具有聚集诱导发光特性,在光电材料领域应用前景广阔,其结构简式如图所示,下列说法正确的是( )
有机物TPE具有聚集诱导发光特性,在光电材料领域应用前景广阔,其结构简式如图所示,下列说法正确的是( )| A. | 该有机物的分子式为C26H22 | |
| B. | 该有机物属于苯的同系物 | |
| C. | 该有机物的一氯代物有4种 | |
| D. | 该有机物既可发生氧化反应,又可发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 )分子中有5n个σ键
)分子中有5n个σ键| 化学键 | Si-Si | O═O | Si-O |
| 键能(kJ•mol-1) | a | b | c |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com