
��12�֣���ش��й������������壺H2��O2��NO��NH3��NO2���� �⡣
I.��1������ȡO2 �ķ���װ����ͬ���ǣ�______________ֻ����һ�ַ����ռ�����______________________________
��2�����������Ʊ���Ӧ��,��һ��Ӧ��ԭ������������Ӧ�����ܹ�Ϊͬһ���ͣ���д��ʵ������ȡ������ķ���ʽ____________________________________________________
II. ����ͼװ�ý�����Ȫʵ�飨ͼ�мг�װ�þ�����ȥ����

��1������ͼ1װ�ý�����Ȫʵ�飬�ϲ���ƿ��װ������İ���������ˮ����IJ�����_____________________��ʵ���ԭ����______________________________________
��2������ͼ2��װ�ã����һ��˵��������Ȫ�ķ���___________________________
III������ͬһ��ƿ�ֱ�����������壺�� HCl �� NH3 �� NO2������Ȫʵ�飬ʵ�����ƿ����ҺҺ��ĸ߶ȹ�ϵΪ____________________________ ������ź͡�>,<��=����ʾ����ͬ����������Һ���ʵ���Ũ�ȴ�С��ϵΪ ____________________________ ��
 ��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���û�ѧ֪ʶ��������������е��й����ⱸ�ܹ�ע����ش��������⣺
���û�ѧ֪ʶ��������������е��й����ⱸ�ܹ�ע����ش��������⣺| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
��6�֣�����˵����ȷ���� ������ţ���
�����ڵ��ھƾ��е��ܽ�ȴ����Կ��þƾ�����ˮ�еĵ���ȡ����
��ˮ�ķе���100�棬�ƾ��ķе���78.5�棬��ֱ��������ʹ��ˮ�ƾ���Ϊ��ˮ�ƾ�
�����ڽ�����ֱ�������Ӵ����Ե�����Һ�л��еĵ⻯�ؿ�������������
�ܷ��뱽�ͱ��ӵĻ��Һ���ȼ�������Ũ��ˮ���ٹ��ˡ���Һ������ʵ��
�����ڸ�֬����������ˮ�еķ�ɢ����ֱ����1nm��100 nm֮�䣬���Կ���ʳ��ʹ��֬�����ɴ�������Ӧ��Ļ����������
�����ѱ�����Һմ��Ƥ���ϣ�Ӧ�����þƾ�ϴ��
����ϡ��ˮ���뱽����Һ���Ʊ�2��4��6�����屽��
��ʵ����ʹ�������Ϊ1:3��Ũ�������Ҵ��Ļ����Һ����ϩʱ��Ϊ������ʱ��Ӧ���Һ���ֱ���������Ҫ�ӷ�ʯ�⣬��Ӧע����������¶���������170��
17��.(18��)ij��ѧС���������������������װ�ã�����ͼ�����Ի������Ʊ�����ϩ��
 ��֪��
��֪��
| �ܶ� | �۵� | �е� | �ܽ��� | |
| ������ | 0.96 | 25 | 161 | ������ˮ |
| ����ϩ | 0.81 | ��103 | 83 | ������ˮ |
��1���Ʊ���Ʒ
��12.5mL�����������Թ�A�У��ټ���1mLŨ���ᣬҡ�Ⱥ�������Ƭ��������������Ӧ��ȫ�����Թ�C�ڵõ�����ϩ��Ʒ��
��A�����Ƭ�������� ��
����B���˵�������е������� ��
���Թ�C���ڱ�ˮԡ�е�Ŀ���� ��
 ��2���Ʊ���Ʒ
��2���Ʊ���Ʒ
�ٻ���ϩ��Ʒ�к��л������������������ʵȡ����뱥��
ʳ��ˮ�������á��ֲ㣬����ϩ�� �㣨��
���ϡ����¡�������Һ���� �������ţ�ϴ�ӡ�
A��KMnO4��Һ B��ϡH2SO4 C��Na2CO3��Һ
���ٽ�����ϩ����ͼװ��������ȴˮ�� �ڽ��롣
����ʱҪ������ʯ�ң�Ŀ����:���� ���� ��
���ռ���Ʒʱ�����Ƶ��¶�Ӧ�� ���ң�ʵ���ƵõĻ���ϩ��Ʒ�����������۲��������ܵ�ԭ���� �� ��
A������ʱ��70�濪ʼ�ռ���Ʒ B��������ʵ����������
C���Ʊ���Ʒʱ���������Ʒһ������
��3���������ֻ���ϩ��Ʒ�ʹ�Ʒ�ķ������������� ( )
A�������Ը��������Һ B���ý����� C���ⶨ�е�
18����12�֣��л�
��A�Ľṹ��ʽΪ![]() ������ͨ����ͬ��ѧ��Ӧ�ֱ��Ƶ�B��C��D��E�������ʡ�
������ͨ����ͬ��ѧ��Ӧ�ֱ��Ƶ�B��C��D��E�������ʡ�

��ش��������⣺
��1��ָ����Ӧ�����ͣ�A��C�� ��
��2����A~E���������У���Ϊͬ���칹����� ������ţ���
��3��д����A����B�Ļ�ѧ����ʽ
��
��4����֪HCHO����������ԭ�Ӷ���ͬһƽ���ڣ������������������е�ԭ���п��ܶ���ͬһƽ��������� ������ţ���
��5��C���γɸ߾���ø߾���Ľṹ��ʽΪ ��
��6��д��D��NaOH��Һ���ȷ�Ӧ�Ļ�ѧ����ʽ
��
19.��16�֣���
��������� �������ڵ��ƾ��в�ݮ�����ѡ�ӣ�ҡ�����������ζ��ʳ���㾫
�������ڵ��ƾ��в�ݮ�����ѡ�ӣ�ҡ�����������ζ��ʳ���㾫
�����������ķ���ʽ�� ��
 �������й����������������У���ȷ���� ����ĸ����
�������й����������������У���ȷ���� ����ĸ����
A������������Ȼ�̼��Һ�����ӳɷ�Ӧ
B����ʹ���Ը��������Һ��ɫ
C���ڼ����������ܷ���ˮ�ⷴӦ
D�������ܷ����Ӿ۷�Ӧ
��GΪ����������һ��ͬ���칹�壬����ӽṹģ������ͼ��ʾ��ͼ��������֮�����߱�ʾ������˫��������G�Ľṹ��ʽΪ ��
���÷�����AΪԭ�Ϻϳ�G��·�����£�

�ٻ�����E�еĹ������� �������ƣ���
��F��G�ķ�Ӧ������ ���÷�Ӧ�Ļ�ѧ����ʽΪ _ _ ��
��C��D�Ļ�ѧ����ʽΪ _��
��д����������������F��ͬ���칹��Ľṹ��ʽ ��O%M
���������ں��������ұ�����ֻ��һ��֧����
����һ�������£�1mol������������������Һ��ַ�Ӧ������4mol�����ʡ�
20����10�֣��л���A��������ͬ��ͬѹ������������ܶ�Ϊ31��ȡ3.1��A���������������г��ȼ�գ�ֻ����2.7��ˮ�ͱ�״����CO22.24L�����л���ķ���ʽ�������л���0.2molǡ����9.2�˽�������ȫ��Ӧ����д���л���Ľṹ��ʽ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���û�ѧ֪ʶ��������������е��й����ⱸ�ܹ�ע����ش��������⣺
��1����֪ˮ��������ƽ�⣺H2O![]() H++OH- ��H>0������ʹƽ�������ƶ�����������Һ�Լ��ԣ�ѡ���� ��
H++OH- ��H>0������ʹƽ�������ƶ�����������Һ�Լ��ԣ�ѡ���� ��
A. ��ˮ�м���NaHSO4���� B. ��ˮ�м�Na2CO3����
C. ������100��[����c(H+) = 1��10-6 mol•L-1] D. ��ˮ�м���NH4Cl����
��2�������£�Ũ�Ⱦ�Ϊ0��1mol��L-1����������������Һ��pH���±���
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8��8 | 9��7 | 11��6 | 10��3 | 11��1 |
��������Һ�е������ӣ����H+������ǿ����_________�����ݱ������ݣ�Ũ�Ⱦ�Ϊ0��01mol��L��1���������������Һ�ֱ�ϡ��100����pH�仯������________�����ţ���
A��HCN B��HClO C��CH3COOH D��H2CO3
��3��ʵ�����г���NaOH������ϴ�����ᴿ����400mL 1mol��L-1��NaOH��Һ���ձ�״����4��48LCO2ʱ��������Һ�и�����Ũ���ɴ�С��˳��Ϊ________________��
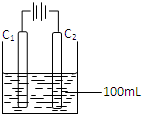
 ��4��ʵ�����в��ö��Ե缫ģ�ҵ�ϵ�ⱥ��ʳ��ˮ�Ĺ��̣�
��4��ʵ�����в��ö��Ե缫ģ�ҵ�ϵ�ⱥ��ʳ��ˮ�Ĺ��̣�
��д��C1�缫�Ϸ�����Ӧ�ĵ缫��Ӧʽ ��
�ڵ�C2�缫�ϲ���112mL(��״��)����ʱ������������ȫ
�ݳ�����Һ������䣩���ձ�����Һ��pH= ����Kw=10-14��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��ɽ��ʡ���������ѧУ�������ϣ����л�ѧ�Ծ��������棩 ���ͣ������
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com