解:(1)黄铜矿与空气反应生成Cu
2S、FeS,根据化合价升降相等配平,反应方程式为:2CuFeS
2+O
2 
Cu
2S+2FeS+SO
2;FeS和氧气反应生成FeO,根据化合价升降相等,配平方程式为:FeS+3O
2 
2FeO+2SO
2,生成炉渣的主要成分为:FeSiO
3,
故答案是:2CuFeS
2+O
2 
Cu
2S+2FeS+SO
2;FeS+3O
2 
2FeO+2SO
2 FeSiO
3;
(2)Cu
2S被氧化为Cu
2O的反应方程式为:2Cu
2S+3O
2 
2Cu
2O+2SO
2;Cu
2O与Cu
2S发生反应的方程式为:2Cu
2O+Cu
2S

6Cu+2SO
2↑,
故答案是:2Cu
2S+3O
2 
2Cu
2O+2SO
2;2Cu
2O+Cu
2S

6Cu+2SO
2↑;
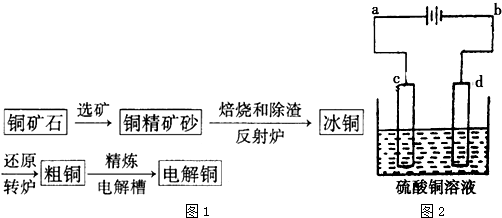
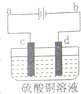
(3)c连电源正极,d连电源的负极;故c为阳极,d为阴极;粗铜板应放在阳极,即c;d阴极发生还原反应,方程式为:Cu
2++2e
-=Cu;Au、Ag比较稳定,不反应,以单质形式沉积在c(阳极)下方,Fe失去电子变成Fe
2+的形式进入电解液中,
故答案是:c;Cu
2++2e
-=Cu;Au、Ag以单质形式沉积在c(阳极)下方,Fe以Fe
2+的形式进入电解液中.
分析:(1)黄铜矿与空气反应生成Cu和Fe的低价硫化物:产物为Cu
2S、FeS;部分Fe的硫化物转变为Fe的低价氧化物:产物为FeO;反射炉内生成炉渣的主要成分是FeSiO
3;
(2)Cu
2S被氧化为Cu
2O:2Cu
2S+3O
2 
2Cu
2O+2SO
2;Cu
2O与Cu
2S反应:2Cu
2O+Cu
2S

6Cu+2SO
2↑;
(3)粗铜应该放在阳极,c是阳极;d是阴极,发生还原反应 Cu
2++2e
-=Cu;粗铜中的Au、Ag、,它们在电解槽中的下方,以单质形式沉积在c(阳极)下方;Fe以Fe
2+的形式进入电解液中.
点评:本题考查铜及其化合物的性质,特别是阅读信息、处理信息的能力,难度稍大.

 Cu2S+2FeS+SO2;FeS和氧气反应生成FeO,根据化合价升降相等,配平方程式为:FeS+3O2
Cu2S+2FeS+SO2;FeS和氧气反应生成FeO,根据化合价升降相等,配平方程式为:FeS+3O2  2FeO+2SO2,生成炉渣的主要成分为:FeSiO3,
2FeO+2SO2,生成炉渣的主要成分为:FeSiO3, Cu2S+2FeS+SO2;FeS+3O2
Cu2S+2FeS+SO2;FeS+3O2  2FeO+2SO2 FeSiO3;
2FeO+2SO2 FeSiO3; 2Cu2O+2SO2;Cu2O与Cu2S发生反应的方程式为:2Cu2O+Cu2S
2Cu2O+2SO2;Cu2O与Cu2S发生反应的方程式为:2Cu2O+Cu2S  6Cu+2SO2↑,
6Cu+2SO2↑, 2Cu2O+2SO2;2Cu2O+Cu2S
2Cu2O+2SO2;2Cu2O+Cu2S  6Cu+2SO2↑;
6Cu+2SO2↑; 2Cu2O+2SO2;Cu2O与Cu2S反应:2Cu2O+Cu2S
2Cu2O+2SO2;Cu2O与Cu2S反应:2Cu2O+Cu2S  6Cu+2SO2↑;
6Cu+2SO2↑;

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案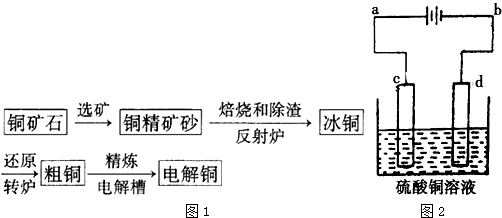
 由黄铜矿(主要成分是CuFeS2)可以冶炼得到粗铜,再经过电解精炼得到纯铜.
由黄铜矿(主要成分是CuFeS2)可以冶炼得到粗铜,再经过电解精炼得到纯铜.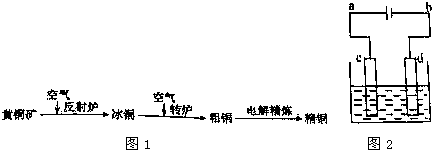
 8Cu+4FeO+2Fe2O3+16SO2若CuFeS2中的Fe的化合价为+2,反应中被还原的元素是______(填元素符号).
8Cu+4FeO+2Fe2O3+16SO2若CuFeS2中的Fe的化合价为+2,反应中被还原的元素是______(填元素符号).