
| A. | 臭氧、乙醇溶液均可用于消毒杀菌且原理完全相同 | |
| B. | 半导体材料和光纤制品都是以硅为基本原料生产的 | |
| C. | 煤的干馏和石油的分馏均属化学变化 | |
| D. | 亚硝酸盐、二氧化硫均可以用作食品的防腐剂 |
分析 A、臭氧有强的氧化性,会将物质氧化有消毒杀菌作用;而乙醇溶液则是使蛋白质分子结构改变,失去生理活性;
B、半导体材料是以晶体硅为原料生产的,而光纤制品是以二氧化硅为基本原料生产的;
C、石油分馏是利用沸点不同分馏混合物的方法;
D、亚硝酸盐有强的氧化性,会使病毒的蛋白质氧化变性;二氧化硫溶于水形成亚硫酸,有抑制微生物生长的作用;二氧化硫有还原作用,可消耗果蔬组织中的氧,可以抑制氧化酶的活性,从而抑制酶性褐变,有抗氧化作用.
解答 解:A、臭氧利用了强氧化性消毒杀菌,乙醇破坏了蛋白质原有的氢键使蛋白质变性,原理不完全相同,故A错误;
B、二氧化硅具有折光性,用于生产光导纤维,硅用于太阳能电池和半导体材料,故B错误;
C、石油分馏是利用沸点不同分馏混合物的方法,为物理变化,而煤干馏是在隔绝空气的条件下,将煤加热到900~1100℃时,可以得到焦炭、煤焦油、煤气等物质,为化学变化,故C错误;
D、亚硝酸盐有强的氧化性,会使病毒的蛋白质氧化变性,因此可以用于食品的防腐;二氧化硫溶于水形成亚硫酸,有抑制微生物生长的作用,可达到食品防腐的目的;二氧化硫有还原作用,可消耗果蔬组织中的氧,可以抑制氧化酶的活性,从而抑制酶性褐变,有抗氧化作用,故D正确;
故选:D.
点评 本题主要考查物质的性质及应用的知识,难度不大,注意相关知识的积累与区分.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙烷与Cl2反应制氯乙烷 | |
| B. | 乙醇和浓硫酸共热制乙烯 | |
| C. | 乙酸和乙醇共热酯化 | |
| D. | 乙烯在催化剂作用下直接氧化制得唯一产物乙醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
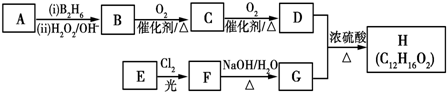
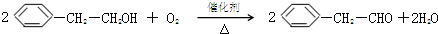 .
. .
.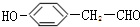 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋除去暖瓶内的水垢 | |
| B. | 鸡蛋白溶液中加入硫酸铵饱和溶液后析出白色沉淀 | |
| C. | 淀粉溶液中加碘水变蓝 | |
| D. | 棉花织品和羊毛织品:分别灼烧闻气味 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,下列关于该物质的说法正确的是( )
,下列关于该物质的说法正确的是( )| A. | 其分子式为C15H21O4 | |
| B. | 分子中只含有两种极性共价键 | |
| C. | 既能发生加聚反应,又能发生酯化反应 | |
| D. | 既能与FeCl3溶液发生显色反应,又能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溴水鉴别苯、四氯化碳、苯乙烯 | |
| B. | 除去苯中少量苯酚,先加浓溴水,再过滤 | |
| C. | 用酸性高锰酸钾溶液洗气,可以除去乙烷气体中乙烯 | |
| D. | 除去乙酸乙酯中的乙酸和乙醇可用氢氧化钠溶液洗涤,再分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com