
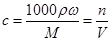 ���������ݿɵó�V="168" mL��
���������ݿɵó�V="168" mL��

 ���ſ����ϵ�д�
���ſ����ϵ�д� ���Ŀ����ϵ�д�
���Ŀ����ϵ�д� ������ӱ������ͯ������ϵ�д�
������ӱ������ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������


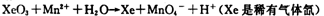


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��2Cl-��Cl2 | B��Fe3+��Fe2+ |
| C��Cu2+��Cu | D��MnO ��MnO2 ��MnO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
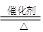 4NO + 6H2O ��������Ϊ��ԭ���������� ���ѧʽ��������Ӧ��������0.2 mol NO����ת�� mol���ӣ�
4NO + 6H2O ��������Ϊ��ԭ���������� ���ѧʽ��������Ӧ��������0.2 mol NO����ת�� mol���ӣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ʯ��ϡ���ᡡ | B����������Һ���Ȼ�����Һ�� |
| C��п����ϡ���ᡡ | D��̼��ˮ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��C12�������� | B��H2SO4���������� |
| C����Ӧ��SԪ�صļ�̬���� | D����Ӧ��H2O������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������Һ | B��������Һ | C������ | D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������ΪFe3+����ԭ��ΪCu2+��S2+ |
| B������������S����ԭ������Fe2+��Cu2+ |
| C����ת��1mol����ʱ����46 g CuFeS2�μӷ�Ӧ |
| D����������������Fe3+��Fe2+��Cu2+ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com