
��ҵ��ˮ�г�����һ������Cr2O ��CrO
��CrO �����ǻ����̬ϵͳ��ɺܴ�������л�ԭ�������dz��õ�һ�ִ����������������£�
�����ǻ����̬ϵͳ��ɺܴ�������л�ԭ�������dz��õ�һ�ִ����������������£�
���еڢٲ��д���ƽ�⣺2CrO (��ɫ)��2H��
(��ɫ)��2H�� Cr2O
Cr2O (��ɫ)��H2O�������й�˵����ȷ����
(��ɫ)��H2O�������й�˵����ȷ����
A���ڢٲ���2v(Cr2O )��v(CrO
)��v(CrO )ʱ���ﵽ��ƽ��״̬
)ʱ���ﵽ��ƽ��״̬
B����������ƽ�⣬��������ϡ�������Һ��ɫ���ɫ����������CrO ������
������
C�������£�Cr��OH��3���ܶȻ�Ksp=10-32��Ҫʹc��Cr3+������10-5mol/L����Һ��pHӦ����9
D���ڢڲ��У���ԭ0.1 mol Cr2O ��Ҫ91.2 g FeSO4
��Ҫ91.2 g FeSO4
D
��������
���������A���ڢٲ���v(Cr2O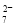 )��2v(CrO
)��2v(CrO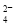 )ʱ���ҷ�Ӧ�������ʱ�ﵽ��ƽ��״̬��A����B����������ϡ�������Һ��ɫ���ɫ��˵��������CrO
)ʱ���ҷ�Ӧ�������ʱ�ﵽ��ƽ��״̬��A����B����������ϡ�������Һ��ɫ���ɫ��˵��������CrO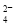 �����ɣ�B����C�������ܶȻ���������ʽ��֪����c��Cr3+����10-5mol/L����Һ��������Ũ����
�����ɣ�B����C�������ܶȻ���������ʽ��֪����c��Cr3+����10-5mol/L����Һ��������Ũ����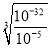 ��10��9mol/L������Һ��pH��5��C����D���ڢڲ��У�CrԪ�ػ��ϼ���+6�۽���Ϊ+3���������ӱ�����Ϊ�����ӣ���ԭ0.1mol Cr2O72-����ת�Ƶ������ʵ�����0.1mol��2����6-3��=0.6mol�����ݵ���ת���غ��֪����ҪFeSO4�����ʵ�����0.6mol��������0.6mol��152g/mol��91.2g����D��ȷ����ѡD��
��10��9mol/L������Һ��pH��5��C����D���ڢڲ��У�CrԪ�ػ��ϼ���+6�۽���Ϊ+3���������ӱ�����Ϊ�����ӣ���ԭ0.1mol Cr2O72-����ת�Ƶ������ʵ�����0.1mol��2����6-3��=0.6mol�����ݵ���ת���غ��֪����ҪFeSO4�����ʵ�����0.6mol��������0.6mol��152g/mol��91.2g����D��ȷ����ѡD��
���㣺����ƽ���ƶ���������ԭ��Ӧ�����������


 С�����ϵ�д�
С�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�����ʡ��ˮ�и߶���ѧ�����п��Ի�ѧ�������Ծ��������棩 ���ͣ�ѡ����
�����£���1.000 mol��L-1�������20.00 mL 1.000 mol��L-1��ˮ�У���ҺpH���¶��������������仯������ͼ��ʾ�������й�˵����ȷ����
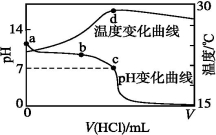
A��a����ˮ�������c(H+)=1��0��10-14 mol��L-1
B��b�㣺c( NH4+)+c(NH3��H2O)=c(Cl-)
C��c�㣺c(Cl-)=c(NH4+)
D��d�����Һ�¶������½�����Ҫԭ����NH3��H2O��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ��ˮ�и߶���ѧ�����п��Ի�ѧ���ģ��Ծ��������棩 ���ͣ�ѡ����
���жԺϽ���������ȷ����
A���Ͻ����ֻ�ܺ�������Ԫ��
B�������Ͻ��Ӳ�Ƚϴ�
C�������Ͻ���۵�ȳɷֽ�����
D���Ͻ�����ܸ��Ͻ�Ԫ�ص������й�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ��ˮ�и�����ѧ�ڵ�һѧ�ο��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й���Ԫ�ؼ��仯�����˵����ȷ����
A��Fe�ڳ����¿���Ũ���ᡢϡ���ᡢŨ������ҷ�Ӧ
B��Al��Cl2���ܺ�NaOH��Һ����������ԭ��Ӧ���������ʵ�������ͬ
C��Na�����ڿ����У����ԺͿ����е��й����ʷ�����Ӧ����������Na2CO3
D���Ʊ�FeCl3��CuCl2������ɲ��ý���Һֱ�����ɵķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ����9���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
��14�֣�����ͼ��ʾװ�ý�������ˮ������Ӧ��ʵ�顣

��1��������ˮ������Ӧ�Ļ�ѧ����ʽ�ǣ� ��
(2)Ϊ�������ɵ��������,�����ͼѡ���Ҫ��װ��,����ȷ������˳��Ϊ(�ýӿ���ĸ��ʾ)
a���� ,������֤����������ʵ������_�� ��

��3��ֹͣ��Ӧ����װ����ȴ��ȡ����Ӧ�������ۻ������������ϡ�����ַ�Ӧ�����ˡ���������������Һ��Fe3���IJ��������� ��
��4��������������Һ�в���Fe3�����ⲻ��˵��������ˮ������Ӧ���ò����в�����3�۵�����ԭ���ǣ��û�ѧ����ʽ˵������ ��
��5��ijͬѧ����������Һ��ȡ��ɫ��Fe��OH��2����������Һ�м���NaOH��Һ�۲쵽���ɵİ�ɫ����Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ��
�ٳ����ɰ�ɫ��Ϊ���ɫ�Ļ�ѧ����ʽ�ǣ� ��
��Ϊ�˵õ���ɫ��Fe��OH��2��������������ʹ������ʱ�䱣�ְ�ɫ����ͬѧ�������ͼ��ʾ��װ�ã�
ͨ�����Һ�в��������İ�ɫ�������ҽϳ�ʱ�䲻��ɫ������˵������ȷ����________(�����)��

A����Դ�е�aΪ������bΪ���� B��������NaCl��Һ��Ϊ���Һ
C��A��B���˶������������缫 D�����������ķ�Ӧ��2H����2e��===H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ����9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�¶��£����һ�����ܱ������н������¿��淴Ӧ��X(g)��Y(g) Z(g)��W(s)����H��0������������ȷ����
Z(g)��W(s)����H��0������������ȷ����
A����������W���淴Ӧ�������� B��������������ѹǿ����ʱ����Ӧ�ﵽƽ��
C�������¶ȣ�ƽ�������ƶ� D��ƽ������X��������Ӧ�ġ�H����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ����9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����H����H2O===H2��OH��˵����ȷ����
A���÷�Ӧ�����û���Ӧ
B�����÷�Ӧ����1 mol����ת�ƣ�������H2��22.4 L
C��ˮ��������
D��H2ֻ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ijϡ��Һ�к���Fe(NO3)3��Cu(NO3)2��HNO3�����������������ۣ���Һ��Fe2��Ũ�Ⱥͼ������۵����ʵ���֮��Ĺ�ϵ����ͼ��ʾ��������1.5mol���۲���ַ�Ӧ�����Һ��Fe(NO3)3��Fe(NO3)2��Cu(NO3)2���ʵ���Ũ��֮��Ϊ( )
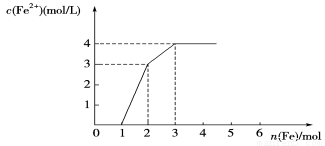
A��1��1��1 B��1��3��1 C��2��3��2 D��1��1��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�����и�����ѧ�ڵڶ���ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
�Ը������������Ĺ�ҵ��ҺΪԭ�������������Ĺ������£����ֲ����������ԣ���
��.�ӷ�Һ���ᴿ���ᾧ��FeSO4��7H2O��
��.��FeSO4��7H2O���Ƴ���Һ��
��.FeSO4��Һ���Թ�����NH4HCO3��Һ��ϣ��õ���FeCO3����Һ��
��.����Һ���ˣ���90����ˮϴ�ӳ����������õ�FeCO3���塣
��.����FeCO3���õ�Fe2O3���塣
��֪��NH4HCO3����ˮ�зֽ⡣
��1�����У�����������м��ȥ��Һ�е�Fe3+���÷�Ӧ�����ӷ���ʽ��_________________��
��2�����У����һ�������ᡣ���û�ѧƽ��ԭ���������������_____________��
��3�����У�����FeCO3�����ӷ���ʽ��_____________����FeCO3��Һ��ʱ�䱩¶�ڿ����У����в��ֹ�������Ϊ���ɫ���ñ仯�Ļ�ѧ����ʽ��_____________��
��4�����У�ͨ������SO42-���жϳ����Ƿ�ϴ�Ӹɾ�������SO42-�IJ�����_____________��
��5����֪����FeCO3�Ļ�ѧ����ʽ��4FeCO3+O2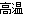 2Fe2O3+4CO2��������464.0 kg��FeCO3,�õ�316.8 kg��Ʒ������Ʒ������ֻ��FeO����ò�Ʒ��Fe2O3��������_________ kg����Ħ������/g��mol-1:FeCO3 116 Fe2O3 160 FeO 72��
2Fe2O3+4CO2��������464.0 kg��FeCO3,�õ�316.8 kg��Ʒ������Ʒ������ֻ��FeO����ò�Ʒ��Fe2O3��������_________ kg����Ħ������/g��mol-1:FeCO3 116 Fe2O3 160 FeO 72��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com