
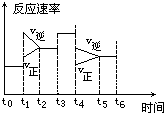
 一密封体系中发生下列反应:N2+3H2 2NH3+Q,下图是某一时间段中反应速率与反应进程的曲线关系图:
一密封体系中发生下列反应:N2+3H2 2NH3+Q,下图是某一时间段中反应速率与反应进程的曲线关系图:

科目:高中化学 来源: 题型:
| A、BaCl2溶液 |
| B、NaOH溶液 |
| C、AgNO3溶液 |
| D、Ba(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C3H8和C3H6 |
| B、C2H6和C3H6 |
| C、C2H4和C4H8 |
| D、CH4和C2H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图:
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图: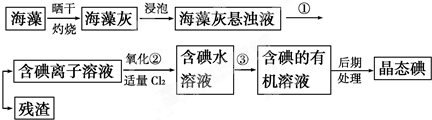
查看答案和解析>>
科目:高中化学 来源: 题型:
| 884消毒液 【有效成分}NaClO 【规格】1 000mL 【质量分数】25% 【密度】1.19g?cm-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度10℃ |
| B、0.1mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度10℃ |
| C、0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度60℃ |
| D、0.2mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度30℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com