
合金是不同金属或金属与一些非金属熔化状态下形成的一种熔合物,根据下表中提供的数据,判断可以形成合金的
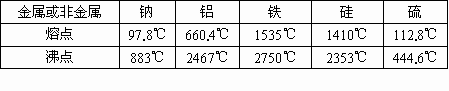
[ ]
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:阅读理解
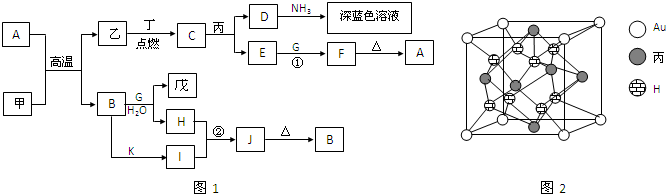




查看答案和解析>>
科目:高中化学 来源: 题型:
| A | |||||||||||||||||
| M | Q | R | |||||||||||||||
| E | D | ||||||||||||||||
| G | J | ||||||||||||||||
查看答案和解析>>
科目:高中化学 来源:活题巧解巧练·高考化学(第一轮) 题型:013
合金是不同金属或金属与一些非金属熔化状态下形成的一种熔合物,根据表1提供的数据,判断可以形成合金的是

[ ]
查看答案和解析>>
科目:高中化学 来源: 题型:022
合金是一类用途广泛的金属材料,合金具有许多优良的______、______或_______性能,在许多方面优于各成分金属。合金的硬度一般比它的各成分金属的________,多数合金的熔点一般也比它的各成分金属的_________。使用不同的________,改变原料的______,变更制造合金的______等,可以制得具有不同性能的合金。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com