
分析 (1)根据同一化合物中各元素的化合价的代数和为0;根据各元素的化合价判断(注意会判断充电时的反应物、生成物的);
(2)电镀时,镀件连接电源的负极,镀层连接电源的正极,阳极发生氧化反应,Ni被氧化生成Ni2+.
解答 解:(1)在化合物中各元素的化合价的代数和为0,在LiNiO2中锂元素的化合价为+1,氧元素的化合价为-2,所以镍元素的化合价为+3;充电时,反应物为LiNiO2,LiNiO2中锂元素的化合价为+1,氧元素的化合价为-2,镍元素的化合价为+3,生成物是Li和Li1-xNiO2,单质镍的化合价为0价,Li1-xNiO2中锂元素的化合价为+1,氧元素的化合价为-2,镍元素的化合价为4+x,所以变化的元素有锂和镍,
故答案为:+3价;Li、Ni;
(2)电镀时,镀件连接电源的负极,镀层连接电源的正极,阳极发生氧化反应,Ni被氧化生成Ni2+,电极方程式为Ni-2e-=Ni2+,故答案为:负极;Ni-2e-=Ni2+.
点评 本题考查原电池和电解池,为高频考点,侧重于学生的分析能力的考查,明确电极上发生的反应是解本题关键,结合物质的性质来分析解答,注意把握元素化合价的判断,难度中等.


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙醇和汽油都是可再生能源,所以要大力发展“乙醇汽油” | |
| B. | 甲基丙烯酸甲酯可以发生加成、水解和氧化反应 | |
| C. | 苯和苯甲酸的混合物1mol,完全燃烧消耗O2的分子数为7.5NA | |
| D. | 乙苯能被酸性KMnO4溶液氧化,是因为苯环对侧链上的-CH2-产生了影响,使其变活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | ||
| C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液和Ca(OH)2溶液 | B. | Na2O和H2O | ||
| C. | Na2SO4溶液和CuCl2溶液 | D. | Na和NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
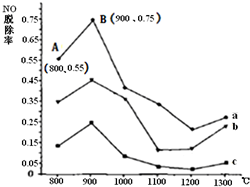 尿素[CO(NH2)2]在一定条件下能有效将NO转化为N2.如图为CO(NH2)2与某种烟气(主要为N2、NO)中NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率(NO的消耗量与NO的原始量的比值)随温度变化的曲线图.
尿素[CO(NH2)2]在一定条件下能有效将NO转化为N2.如图为CO(NH2)2与某种烟气(主要为N2、NO)中NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率(NO的消耗量与NO的原始量的比值)随温度变化的曲线图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1Na2CO3溶液中,c(OH)-=c(H+)+c(HCO3-)+c(H2CO3) | |
| B. | 相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则对于同温、同体积、同pH的HCN和HClO分别与Na0H恰好完全反应时,消耗NaOH的物质的量:HClO<HCN | |
| C. | 向醋酸钠溶液中加入适量醋酸,得到酸性的混合溶液:c(Na+)>c(CH3COO-)>C(H+)>c(OH-) | |
| D. | 向硝酸钠溶液中滴加稀盐酸得到pH=5的混合溶液:c(Na+)=c(NO3-)+c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 反应物 | 甲 | 乙 | 丙 |
| A | 2 | 1 | 1 |
| B | 1 | 2 | 1 |
| A. | A的转化率甲<丙<乙 | B. | A的转化率甲<乙<丙 | ||
| C. | B 的转化率甲>丙>乙 | D. | B的转化率甲<乙<丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com