
科目:高中化学 来源:不详 题型:判断题
 )。
)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②③ | C.③④ | D.①④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 □Cu2++□Fe2++□( )+□SO42-
□Cu2++□Fe2++□( )+□SO42-查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ①
①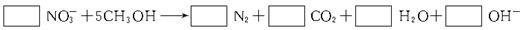
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Si+2CO↑,下列说法正确的是
Si+2CO↑,下列说法正确的是| A.SiO2是氧化剂 | B.SiO2发生氧化反应 |
| C.C表现出氧化性 | D.C被还原 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题




 (1)请完成该化学方程式并配平(未知物化学式和化学计量数填入框内)
(1)请完成该化学方程式并配平(未知物化学式和化学计量数填入框内) (2)浓盐酸在反应中显示出来的性质是 (填写编号)
(2)浓盐酸在反应中显示出来的性质是 (填写编号) ①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com