
【题目】铅蓄电池的充放电总反应为:PbO2 + 2H2SO4 + Pb![]() 2 PbSO4 + 2H2O 下列说法正确的是
2 PbSO4 + 2H2O 下列说法正确的是
A.在放电时,该电池正极上的金属铅被还原
B.在放电时,负极发生的反应是 Pb + SO42--2e-=PbSO4
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是 PbSO4 + 2e-=Pb + SO42-
【答案】B
【解析】
由总方程式可知,为原电池时,Pb为负极,发生氧化反应,电极方程式为Pb+SO42--2e-=PbSO4,PbO2为正极,发生还原反应,电极方程式为PbO2+4H++SO42-+2e-=2H2O+PbSO4。在充电时,阴极发生的反应是PbSO4+2e-=Pb+SO42-,阳极反应为PbSO4-2e-+2H2O=PbO2+SO42-+4H+,放电时,阴离子向负极移动,阳离子向正极移动。
A.在放电时,该电池正极上的氧化铅得电子,被还原,A错误;
B.放电时,Pb为负极,发生氧化反应,电极方程式为Pb+SO42--2e-=PbSO4,B正确;
C.由充电的总反应方程式:2PbSO4+2H2O=PbO2+2H2SO4+Pb,可知充电时,硫酸的浓度增大,C错误;
D.充电时,阳极反应为PbSO4-2e-+2H2O=PbO2+SO42-+4H+,D错误。
答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某课外小组研究铝土矿中A12O3的含量。查阅资料得知,铝土矿的主要成分是A12O3 ,杂质是Fe2O3、SiO2等。从铝土矿中提取A12O3的过程如下:
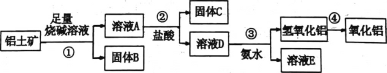
(1)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式是:______。
(2)第②步用到的分离方法是_______。
(3)请从下面仪器中选出第④步操作不需要的仪器_____________(填字母)
A.蒸发皿 B.玻璃棒 C.泥三角 E.酒精灯 F.坩埚
(4)将实验过程中所得固体准确称量。课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中A12O3 的质量分数__________(结果保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况正确的是( )

A. 含0.01 mol NaOH和0.01 mol Ba(OH)2的混合溶液中缓慢通入CO2
B. KHCO3溶液中逐滴加入Ba(OH)2溶液
C. KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液
D. 向含有少量氢氧化钠的偏铝酸钠溶液中滴加盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn(s,白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1
②Sn(s,灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2
③Sn(s,灰)![]() Sn(s,白) △H3=+2.1kJmol-1
Sn(s,白) △H3=+2.1kJmol-1
下列说法正确的是( )
A.△H1>△H2
B.锡在常温下以灰锡状态存在
C.灰锡转为白锡的反应是放热反应
D.锡制器皿长期处在低于13.2℃的环境中,会自行毁坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探索工业废料的再利用,某化学兴趣小组设计了如图实验方案,用含有铝、铁和铜的合金制取氯化铝、绿矾晶体(FeSO47H2O)和胆矾晶体。
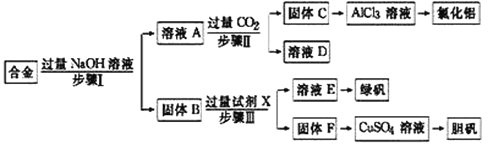
请回答:
(1)步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是_______________。实验室中进行该操作时,用到的玻璃仪器有烧杯、______________________。
(2)溶液A中的阴离子主要有__________________;由合金生成A溶液的离子方程式为:_______________。试剂X是________________。
(3)向溶液A中通入过量CO2气体生成固体C的离子方程式为_________________。
(4)从环境保护角度考虑,采用固体F加入足量稀硫酸里加热并鼓入空气来制备CuSO4溶液,其化学方程式是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和热的测定实验的关键是要比较准确地配制一定的物质的量浓度的溶液,在实验过程中要尽量避免热量的散失,要求比较准确地测量出反应前后溶液温度的变化。回答下列问题:
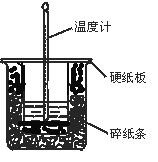
(1)从实验装置上看,图中尚缺少的一种玻璃用品是______________________。
(2)在大小烧杯之间填满碎泡沫(或纸条)其作用是____________________;大烧杯上如不盖硬纸板,求得的中和热数值__________(填“偏大、偏小、无影响”)。
(3)做一次完整的中和热实验,温度计需要使用______次;
(4)该实验常用0.50 mol·L-1HCl和0.55 mol·L-1的NaOH溶液各50 mL。若上述HCl、NaOH溶液的密度都近似为1 g/cm3,中和后生成的溶液的比热容c=4.18 J/(g·℃),反应后温度升高了△t,则生成1mol水时的反应热ΔH=___________ kJ/mol(填表达式)。
(5)如果用50mL0.50mol/L醋酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量______(填“相等、不相等”),简述理由____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向10 mL 0.1000 mol·L-1 NaOH溶液中逐滴加入0.1000 mol·L-1 的某一元酸HX,溶液pH变化曲线如图。下列说法不正确的是
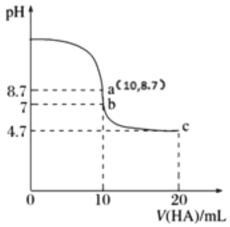
A.等浓度的 HX、NaX 混合溶液中,HX的电离程度大于X- 的水解程度
B.c点所示溶液中存在:2c(H+) - 2c(OH-) = c(X-) - c(HX)
C.a、b、c点所示溶液中,由水电离出的 c(H+)·c(OH-) 值不变
D.a →c点所示溶液中,c(X-) + c(HX) + c(Na+) = 0.1000 mol·L-1 始终成立
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验仪器,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。

(1)A是制取CO2的装置,写出A中发生反应的离子方程式______________。
(2)填写表中空格:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | _____________ |
C | ___________ | _______________ |
D | NaOH溶液 | _____________ |
(3)写出过氧化钠与二氧化碳反应的化学方程式______________________。
(4)用_______________检验F中收集到的气体,现象是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)B的结构简式为______,D 的化学名称为______。
(2)①和③的反应类型分别为______、______。
(3)E的结构简式为______。用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气_______mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中3种的结构简式_______________________________。
(6)写出用2苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com