
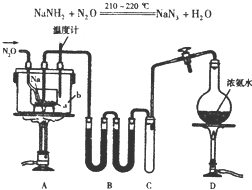
 NaN3(叠氮化钠)是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气囊中的药剂.实验室制取叠氮化钠的原理、实验装置及步骤如下:
NaN3(叠氮化钠)是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气囊中的药剂.实验室制取叠氮化钠的原理、实验装置及步骤如下:分析 (1)反应过程中会产生NaOH,腐蚀玻璃;
(2)制备的氨气中含有大量的水,用C冷凝分离出水,B中盛放碱石灰干燥氨气;
(3)加热时空气中的氧气等能与钠反应,用氨气排尽装置中的空气;步骤②制备NaNH2,还生成氢气;
(4)水的沸点为100℃,不能达到控制的温度;
(5)N2O可由NH4NO3在240-245℃分解制得,反应还生成水,利用待定系数法结合原子守恒配平;
(6)NaN3不溶于乙醚,减少晶体的损失,有利于产品快速干燥;
(7)NaN3与NaClO溶液反应转化为N2,氯元素被还原生成氯化钠.
解答 解:(1)反应过程中有水生成,会反应生成NaOH腐蚀玻璃,
故答案为:反应过程可能生成的NaOH能腐蚀玻璃;
(2)制备的氨气中含有大量的水,用C装置冷凝分离出水,B中盛放碱石灰干燥氨气,
故答案为:碱石灰;冷凝分离出水;
(3)用氨气排尽装置中的空气,防止加热时空气中的氧气等能与钠反应,步骤②制备NaNH2,还生成氢气,反应方程式为:2Na+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$2NaNH2+H2,
故答案为:排尽装置中的空气;2Na+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$2NaNH2+H2;
(4)水的沸点为100℃,不能达到反应控制的温度210一220℃,故用油浴加热,
故答案为:水的沸点为100℃,不能达到反应控制的温度210一220℃;
(5)N2O可由NH4NO3在240-245℃分解制得,反应还生成水,反应方程式为:NH4NO3$\frac{\underline{\;240-245℃\;}}{\;}$N2O↑+2H2O↑,
故答案为:NH4NO3$\frac{\underline{\;240-245℃\;}}{\;}$N2O↑+2H2O↑;
(6)NaN3不溶于乙醚,减少晶体的损失,有利于产品快速干燥,
故答案为:减少晶体的损失,有利于产品快速干燥;
(7)NaN3与NaClO溶液反应转化为N2,氯元素被还原生成氯化钠,
故答案为:NaCl.
点评 本题考查物质的制备、对原理与装置的分析评价、基本操作、信息获取与迁移运用,是对学生综合能力的考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | SO2通入H2S溶液中 | B. | Cl2通入NaOH溶液 | ||
| C. | SO2通入KOH溶液中 | D. | H2S通入溴水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 在稀硫酸中加铜片 | 无明显变化 |
| Ⅱ | 在硝酸钠溶液中加入铜片 | 无明显变化 |
| Ⅲ | 在稀硫酸中加入硝酸钠溶液 | 无明显变化 |
| 再加入铜片 | 有无色气泡;溶液变蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验次数 | V(NaOH) | V(HCl)/mL | c(NaOH) | ||
| ml | 初读数 | 终读数 | 体积 | mol/L | |
| 1 | 16.00 | 0.00 | 16.70 | 16.70 | 0.1044 |
| 2 | 16.75 | 0.00 | 17.85 | 17.85 | |
| 3 | 19.55 | 0.00 | 20.80 | 20.80 | 0.1064 |
| 4 | 15.00 | 0.00 | 16.00 | 16.00 | 0.1067 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
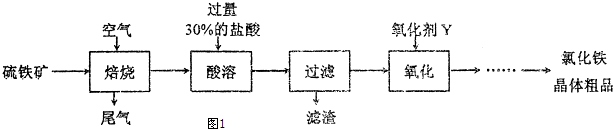
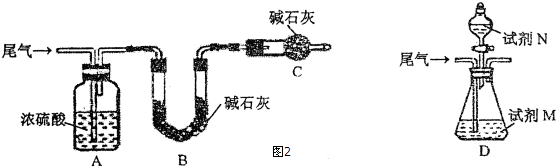
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝与稀盐酸的反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 | ||
| C. | 灼热的碳与二氧化碳的反应 | D. | NaOH与HCl的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
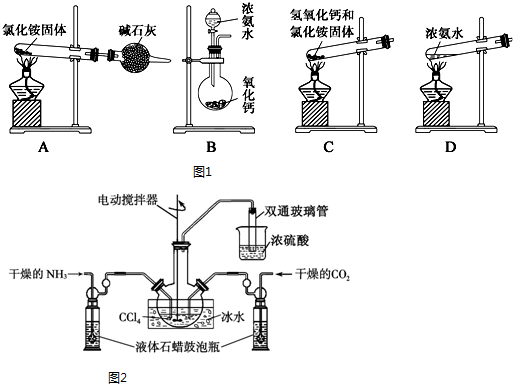
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr;写出B盛AgNO3溶液的试管中所发生反应的化学方程式:HBr+AgNO3=AgBr↓+HNO3.
+HBr;写出B盛AgNO3溶液的试管中所发生反应的化学方程式:HBr+AgNO3=AgBr↓+HNO3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com