
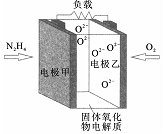
 如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池,该固体氧化物电解质在700-900℃温度时,O2-可在该固体氧化物电解质中自由移动,电池反应生成均为无毒无害的物质,下列说法正确的是( )
如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池,该固体氧化物电解质在700-900℃温度时,O2-可在该固体氧化物电解质中自由移动,电池反应生成均为无毒无害的物质,下列说法正确的是( )| A. | 电池内的由O2-电极乙移向电极甲 | |
| B. | 电池的总反应为:N2H4+2O2═2NO+2H2O | |
| C. | 当甲电极上有1molN2H4消耗时,乙电极上有1molO2被氧化 | |
| D. | 电池外电路的电子由电极乙移向电极甲 |
分析 该燃料电池中,负极上燃料失电子发生氧化反应,电极反应式为:N2H4+2O2--4e-=N2↑+2H2O,正极上氧气得电子发生还原反应,电极反应式为:O2+4e-=2O2-,电池总反应为:N2H4+O2=N2↑+2H2O,结合离子的移动方向、电流的方向分析解答.
解答 解:A.放电时,阴离子向负极移动,即O2-由电极乙移向电极甲,故A正确;
B.反应生成物均为无毒无害的物质,负极上反应生成氮气,则电池总反应为:N2H4+O2=N2↑+2H2O,故B错误;
C.由电池总反应为:N2H4+O2=N2↑+2H2O可知,当甲电极上有1molN2H4消耗时,乙电极上有1molO2被还原,故C错误;
D.电池外电路的电子由负极移向正极,所以由电极甲移向电极乙,故D错误;
故选A.
点评 本题考查了燃料电池,明确正负极上发生的反应是解本题关键,难点是电极反应式的书写,要结合电解质的性质书写,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | MnO2+4HCl(浓)→MnCl2+Cl2↑+2H2O | |
| B. | Ag+2HNO3(浓)→AgNO3+NO2↑+H2O | |
| C. | C+2H2SO4(浓)→CO2↑+2SO2↑+2H2O | |
| D. | 3Fe3O4+28HNO3(浓)→9Fe(NO3)3+NO↑+14H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol的铁与足量的稀硝酸反应,生成气体的分子数目为0.3 NA | |
| B. | 常温常压下,14 g由 C2H4、C3H6组成的混合气体中含有碳原子的数目为NA | |
| C. | 2.24 L CO2与足量的Na2O2反应,转移的电子总数必为0.1NA | |
| D. | l Ll mol/L的KAl(SO4)2溶液中阳离子总数为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,排水法收集气体 | HX放出的氢气多 | HX酸性比HY弱 |
| B | 先向2mL0.15mol•L-1 Na2S溶液中滴几滴0.15mol•L-1 ZnSO4溶液,再加入几滴0.1mol•L-1 CuSO4溶液 | 开始有白色沉淀生成;后又有黑色沉淀生成 | Ksp(ZnS)<Ksp(CuS) |
| C | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 向紫色石蕊试液中持续长时间通入氯气 | 溶液先变红,最后变为无色 | 氯气有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体粒子带电,溶液溶质粒子不带电 | |
| B. | 渗析实验可以鉴别胶体和溶液 | |
| C. | 胶体与溶液都可以通过滤纸、半透膜和分子筛 | |
| D. | 丁达尔效应可以区分胶体和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
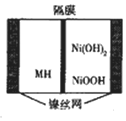 一种新型金属氢化物镍电池(MH-Ni电池,MH为贮氢材料)工作原理如图所示.下列有关说法正确的是( )
一种新型金属氢化物镍电池(MH-Ni电池,MH为贮氢材料)工作原理如图所示.下列有关说法正确的是( )| A. | 隔膜为阴离子交换膜 | |
| B. | 电池的电解液可为硫酸 | |
| C. | 充电时阳极反应为H2O+M+e-═MH+OH- | |
| D. | 放电时负极反应为Ni(OH)2+OH--e-═NiOOH+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.6g乙醇含有的C-H键数为0.6NA | |
| B. | 2gD216O含有的质子数和中子数均为NA | |
| C. | 每生成1molO2,转移的电子数一定为4NA | |
| D. | 标准状况下,22.4L NO与11.2L O2充分反应,产物分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
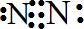 ;将空气中的氮气转化为氮的化合物的过程称为固氮,下列能实现人工固氮的是D
;将空气中的氮气转化为氮的化合物的过程称为固氮,下列能实现人工固氮的是D查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com