
| A、常温下,10mL 0.2mol/L NH4NO3溶液与10mL 0.1mol/L NaOH溶液混合后所得pH=9.6的溶液中:c(NO3-)>c(NH4+)>c(Na+)>c(NH3?H2O)>c(OH-)>c(H+) |
| B、0.1mol/L Na2S溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
| C、常温下a mL 0.1mol/L KOH与b mL 0.1mol/L HCN两溶液混合后pH>7,则一定有a≥b |
| D、10mL 0.1mol/L NaCl溶液中离子总数为x,10mL 0.1mol/L CH3COONa溶液中离子总数为y,则x=y |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、如果ab=cd,则反应后溶液的pH>7 |
| B、如果a=c,且反应后溶液的pH<7,则b<d |
| C、如果a=c、b=d,则反应后的溶液中c(CH3COO-)<c(Na+) |
| D、如果反应后溶液的pH=7,则此溶液中c(CH3COO-)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
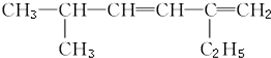
| A、2-甲基-5-乙基-3,5己二烯 |
| B、2-乙基-1,3-己二烯 |
| C、6-甲基-3,4-庚二烯 |
| D、5-甲基-2-乙基-1,3-己二烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相邻的原子之间的相互作用叫做化学键 |
| B、金属和非金属元素的相互化合,都能形成离子键 |
| C、非金属元素的原子半径比其离子半径小(氢除外),金属元素的原子的原子半径比其离子半径大 |
| D、甲元素原子半径比乙元素原子半径大,则甲的离子半径一定比乙的原子半径大 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、生成该聚合物的反应属于加聚反应 |
| B、该聚合物的单体是丙酸乙酯 |
| C、该聚合物分子中存在大量的-OH,所以具有较好的亲水性 |
D、该聚合物的结构筒式为: |
查看答案和解析>>
科目:高中化学 来源: 题型:
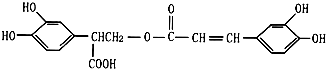
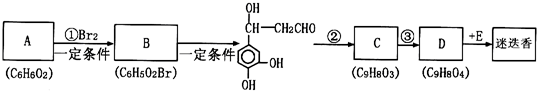
查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:


 )的一条路线如下:
)的一条路线如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应中肼作还原剂 |
| B、此情况下,液态肼燃烧生成1molN2时放出的热量为641.6kJ |
| C、肼(N2H4)分子中只存在极性共价键 |
| D、该反应的反应物总能量高于生成物的总能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com