
| A.用烧碱溶液吸收少量二氧化硫 :SO2 + OH-= HSO3- |
| B.用FeCl3溶液腐蚀铜线路板:Cu + Fe3+= Cu2+ + Fe2+ |
| C.将氯气溶于水制备次氯酸:Cl2 + H2O = 2H+ + Cl- + ClO- |
D.用惰性电极电解饱和氯化钠溶液:2Cl- + 2 H2O 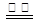 H2↑+ Cl2↑+ 2OH- H2↑+ Cl2↑+ 2OH- |
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.向明矾溶液中加入过量的氢氧化钡溶液: Al3+ + 2SO42-+ 2 Ba2+ + 4OH-= AlO2- + 2BaSO4↓+ 2H2O |
| B.向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+ = Fe2++2H2O |
| C.向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:NH4++OH-=NH3?H2O |
| D.向CH2BrCOOH中加入足量的氢氧化钠溶液并加热: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
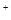 ="===" 2Fe
="===" 2Fe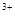 + 3H2↑
+ 3H2↑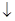
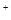 + 2OH
+ 2OH + H2↑
+ H2↑查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铁和稀盐酸反应 2Fe+6H+===2Fe3++3H2↑ |
| B.硝酸银溶液中加入铜粉 Ag++Cu===Cu2++Ag |
| C.氧化铜与盐酸反应 O2― +2H+ ===H2O |
D.碳酸镁跟稀硫酸反应:MgCO3+2H+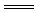 Mg2++H2O+CO2↑ Mg2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向盐酸中滴加氨水:H+ + OH- = H2O |
| B.Fe(OH)3溶于氢碘酸:Fe(OH)3 + 3H+ = Fe3+ + 3H2O |
| C.铜溶于稀硝酸:3Cu + 8H+ + 2NO3- = 3Cu2+ + 2 NO ↑+ 4H2O |
| D.向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硫酸与氢氧化钡溶液反应:Ba2++OH-+SO42—+H+=BaSO4↓+H2O |
| B.用FeCl3溶液腐蚀印刷电路板:Cu+Fe3+=Fe2++Cu2+ |
| C.盐酸与碳酸钡反应: CO32-+2H+==CO2↑+H2O |
| D.硫酸铜溶液中滴加氢氧化钡溶液:Ba2++2OH-+Cu2++SO42-==BaSO4↓+Cu(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.硫酸与氢氧化钡在溶液中反应:Ba2++SO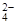 = BaSO4↓ = BaSO4↓ |
| B.用Cl2将苦卤中的Br—氧化:Cl2 +2Br—= 2Cl—+ Br2 |
C.BaCO3与盐酸反应: CO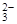 +2H+ = H2O+CO2↑ +2H+ = H2O+CO2↑ |
| D.少量金属钠投入到CuSO4溶液中: 2Na+Cu2+= 2Na++Cu↓ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 烧碱溶液反应:______________________________________
烧碱溶液反应:______________________________________查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CuSO4溶液与Ba(OH)2溶液混合:Ba2++ SO42-= BaSO4↓ |
| B.NaHCO3溶液与稀硫酸混合:HCO3-+ H+= H2O + CO2↑ |
| C.NaHSO3溶液与NaHSO4溶液混合:HSO3-+ HSO4-= SO42-+ H2O + SO2↑ |
| D.Ca(OH)2溶液中通入过量CO2:Ca2++ 2OH-+ CO2 = CaCO3↓+ H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com