
下列离子组在一定条件下能共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是
| 选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
| A | Fe2+、NO、K+ | 稀硫酸 | 3Fe 2++NO+4H+===3Fe3++NO↑+2H2O |
| B | Fe3+、I-、ClO- | 氢氧化钠溶液 | Fe3++3OH-===Fe(OH)3↓ |
| C | Ba2+、HCO、Cl- | 氢氧化钠溶液 | HCO+OH-===CO |
| D | Al3+、Cl-、NO | 过量氢氧化钠溶液 | Al3++3OH-===Al(OH)3↓ |
 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
下列说法或表达正确的是( )
①活性炭、SO2和HClO都具有漂白作用,且漂白的化学原理相同
②向100 mL0.1 mol/L的溴化亚铁溶液中通入0.05 mol的氯气时发生反应的离子方程式:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
③斜长石KAlSi3O8的氧化物形式可表示为:K2O•Al2O3•3SiO2
④酸性条件下KIO3溶液与KI溶液发生反应生成I2时的离子方程式:
IO3-+5I-+3H2O=I2+6OH-
⑤碳酸氢根离子的电离方程式可表示为:

⑥元素周期表中,从上到下,卤族元素的非金属性逐渐减弱,氢卤酸的酸性依次减弱
⑦500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 
 2NH3(g) △H= 38.6 kJ·mol-1
2NH3(g) △H= 38.6 kJ·mol-1
A.全部 B.②⑤ C.②③④⑦ D.②④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质分类正确的是
A.液氯、冰水混合均为纯净物 B.NO2、CO、CO2均为酸性氧化物
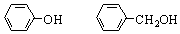 C. 与 互为同系物
C. 与 互为同系物
D.淀粉、纤维素和油脂都属于天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)分别取W g钠、镁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是________。
(2)分别取0.1 mol钠、镁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是________。
(3)若产生相同物质的量的氢气,所需钠、镁、铝的质量比为________。
(4)若产生相同体积(同温同压下)的氢气,所需钠、镁、铝的物质的量比为________。
(5)若将0.2 mol钠、镁、铝分别投入到10 mL 1 mol·L-1的盐酸中,在标准状况下,产生氢气体积的大小顺序是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
质量分数为a%,物质的量浓度为c mol/L 的KOH溶液,蒸发溶剂,恢复到原温度,若质量分数变为2a%,则物质的量浓度变为 ( )
A.大于2c mol/L B.等于2c mol/L
C.小于2c mol/L D.在c mol/L-2c mol/L之间
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关Fe2(SO4)3溶液的叙述正确的是( )
A.该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存
B.和KI溶液反应的离子方程式:
Fe3++2I-===Fe2++I2
C.和Ba(OH)2溶液反应的离子方程式:Fe3++SO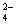 +Ba2++3OH-===Fe(OH)3↓+BaSO4↓
+Ba2++3OH-===Fe(OH)3↓+BaSO4↓
D.1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
氮氧化铝(AlON)是一种透明高硬度防弹材料,可以由反应Al2O3+C+N2=2AlON+CO(高温)合成,下列有关说法正确的是
A.氮氧化铝中氮的化合价是-3
B.反应中氮气作氧化剂
C.反应中每生成5.7g AlON 同时生成1.12 L CO
D.反应中氧化产物和还原产物的物质的量之比是2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有机物的分离提纯方法正确的是
A、除去乙酸乙酯中含有的乙酸杂质,可以加氢氧化钠溶液充分振荡后,分液。
B、用重结晶的方法分离苯甲酸和氯化钠的混合物
C、将工业酒精直接蒸馏可以获得无水酒精
D、用酸性高锰酸钾溶液可以除掉甲烷中的乙烯杂质。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com