
���� ��1������ȶ�����ֽ����ɶ���������ˮ��������
��2����������������һ��������ˮ��
��3��п��ϡ���ᷴӦ��������狀�����п��ˮ��
��4�������������������߷�Ӧ����̼��ơ�̼���ƺ�ˮ��
��5��Cu2S��ϡ���ᷴӦ��������ͭ�����ᡢһ��������ˮ������������ԭ��Ӧ��ʧ�����غ㡢ԭ�Ӹ����غ���д��ѧ����ʽ��
��� �⣺��1������ȶ�����ֽ����ɶ���������ˮ����������ѧ����ʽ��4HNO3 $\frac{\underline{\;����\;}}{\;}$4NO2��+O2��+2H2O��
�ʴ�Ϊ��4HNO3 $\frac{\underline{\;����\;}}{\;}$4NO2��+O2��+2H2O��
��2����������������һ��������ˮ����ѧ����ʽ��4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
�ʴ�Ϊ����������������һ��������ˮ��
��3��п��ϡ���ᰴ���ʵ�����2��5��Ӧ�����ӷ���ʽ��4Zn+10H++NO3-=NH4++4Zn2++3H2O��
�ʴ�Ϊ��4Zn+10H++NO3-=NH4++4Zn2++3H2O��
��4�������������������߷�Ӧ����̼��ơ�̼���ƺ�ˮ�����ӷ���ʽ��Ca2++2OH-+2HCO3-=CaCO3��+CO32-+2H2O��
�ʴ�Ϊ��Ca2++2OH-+2HCO3-=CaCO3��+CO32-+2H2O��
��5��Cu2S��ϡ���ᷴӦ��������ͭ�����ᡢһ��������ˮ����Ӧ�ķ���ʽ��3Cu2S+22HNO3=6Cu��NO3��2+3H2SO4+10NO��+8H2O��
�ʴ�Ϊ��3Cu2S+22HNO3=6Cu��NO3��2+3H2SO4+10NO��+8H2O��
���� ���⿼�������ӷ���ʽ����ѧ����ʽ����д����ȷ��Ӧʵ�ʼ����ӷ���ʽ��д�ǽ���ؼ���ע�����ӷ�Ӧ��ѭ����ʵ����ѭ����غ㡢ԭ�Ӹ����غ���ɣ���Ŀ�ѶȲ���


 ������ȫ��������ϵ�д�
������ȫ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
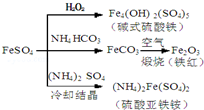
| A�� | ��ʽ������ˮ���ܲ���Fe��OH��3���壬��������ˮ�� | |
| B�� | Ϊ��ֹNH4HCO3�ֽ⣬����FeCO3���ڽϵ��¶��½��� | |
| C�� | ����KSCN��Һ���飨NH4��2Fe��SO4��2�Ƿ����� | |
| D�� | �����£���NH4��2Fe��SO4��2��FeSO4������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
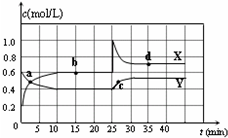 ��֪NO2��N2O4�����ת����2NO2��g��?N2O4��g����H��0���ں��������½�һ����NO2��N2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������У���Ӧ��Ũ����ʱ��仯��ϵ��ͼ������˵����ȷ���ǣ�������
��֪NO2��N2O4�����ת����2NO2��g��?N2O4��g����H��0���ں��������½�һ����NO2��N2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������У���Ӧ��Ũ����ʱ��仯��ϵ��ͼ������˵����ȷ���ǣ�������| A�� | ͼ��Y�����DZ�ʾNO2Ũ����ʱ��ı仯���� | |
| B�� | ǰ10 min��v��N2O4��Ϊ0.1 mol/�� L•min�� | |
| C�� | 25 minʱ������ƽ���ƶ���ԭ���ǽ��ܱ������������СΪ1L | |
| D�� | 25 minʱ������ƽ���ƶ���ԭ����������ͨ������NO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1LCO2�к���3NA��ԭ�� | |
| B�� | 1molCl2����1NA��ԭ�� | |
| C�� | 23g����������Cl2�з�Ӧ��ת�Ƶ�����NA�� | |
| D�� | ������1.00L1.00mol•L-1��NaCl��Һ���ɽ�58.5gNaCl����1.00Lˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��NH4+��=c��Cl-����NH4Cl�Ͱ�ˮ�Ļ����Һ | |
| B�� | c��H+��=1.0��10-7mol•L-1����Һ | |
| C�� | pH=7����Һ | |
| D�� | �����½�pH=3������pH=11�ļ�������Ϻ����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Al��OH��3 | Fe��OH��2 | Fe��OH��3 | |
| ��ʼ����ʱ | 3.4 | 6.3 | 1.5 |
| ��ȫ����ʱ | 4.7 | 8.3 | 2.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
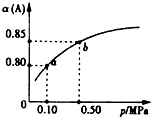 һ���¶��£����ݻ�Ϊ1L���ܱ������м���0.5molA��0.25molB��������Ӧ��2A��g��+B��g��?2C���������ﵽƽ��ʱ���ų�����Q1kJ�������¶Ȳ��䣬A��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ��������˵����ȷ���ǣ�������
һ���¶��£����ݻ�Ϊ1L���ܱ������м���0.5molA��0.25molB��������Ӧ��2A��g��+B��g��?2C���������ﵽƽ��ʱ���ų�����Q1kJ�������¶Ȳ��䣬A��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ��������˵����ȷ���ǣ�������| A�� | ��������������ܶȱ��ֲ��䣬˵����Ӧһ���ﵽƽ��״̬ | |
| B�� | ������ͬ�����£���Ϊֻ����0.5 mol C����Ӧ�ﵽƽ�ⷴ���ų�����Q1kJ | |
| C�� | ƽ��״̬��a�䵽bʱ����ѧƽ�ⳣ��K��a��=K��b�� | |
| D�� | ��ͼ���֪������Cһ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ��ѧ�ĺ�����Ӧ�û�ѧԭ���Ի�����Ⱦ�������� | |
| B�� | PM2.5��������������������ж��к����ʣ����˵ķι�����ɺܴ�Σ�� | |
| C�� | ��������㷺Ӧ����̫���ܵ�ء������оƬ | |
| D�� | ����β���к��д���������Ⱦ��������Ͳ���ȫȼ����ɵ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com