
分析 在水溶液中能够发生部分电离的电解质属于弱电解质,常见的弱电解质包括弱酸、弱碱、少部分的盐和水;
完全电离的电解质属于强电解质,常见的强电解质包括强酸、强碱、大部分的盐,据此分析.
解答 解:①水只能部分电离,故为弱电解质;
②氨水是混合物,既不是电解质也不是非电解质;
③醋酸只能部分电离,故为弱电解质;
④硫酸钠能完全电离,故为强电解质;
⑤氯化银能完全电离,故为强电解质;
⑥氢气是单质,既不是电解质也不是非电解质.
故属于强电解质的而是④⑤;属于弱电解质的是①③.
故答案为:④⑤;①③.
点评 本题考查了常见的强电解质和弱电解质,应注意的是强弱电解质均属于电解质,而电解质必须是化合物,故单质和混合物既不是强电解质也不是弱电解质.


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:解答题
| 元 素 | Mn | Fe | |
| 电离能 (kJ•mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
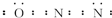 ,其分子空间构型是直线形.
,其分子空间构型是直线形.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | C-C | C-H | H-H | C-O | C=O | H-O |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | 750 | 463 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
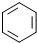 )与苯的真实结构不相符的是BCD.
)与苯的真实结构不相符的是BCD. .
.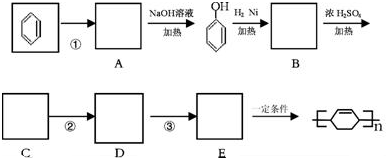
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | A | B | C |
| 结构信息 | 基态原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有1对成对的p电子 | 基态原子核外电子排布为[Ar]3s104sx,有+1、+2两种常见化合价 |
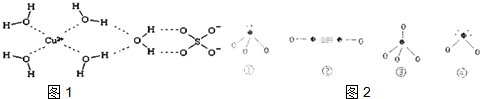
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
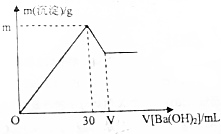 现有10mL1mol/LAl2(SO4)3溶液,向其中逐滴滴加一定物质的量浓度的Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.(已知:Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O)
现有10mL1mol/LAl2(SO4)3溶液,向其中逐滴滴加一定物质的量浓度的Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.(已知:Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com