
����Ŀ���±�Ϊ��ʽ���ڱ���һ���֣����еı�Ŵ�����Ӧ��Ԫ�ء�

��1������λ��ds����Ԫ����________�����ţ���д����Ԫ�ػ�̬ԭ�ӵĵ����Ų�ʽ��___________��
��2���������γɵĻ���������У�����ԭ�ӵ��ӻ��������Ϊ________�������γɵĻ�����ľ���������________��
��3����������������Ԫ���У���һ������������________�����ţ���
��4��Ԫ�����ļ���̬�⻯����ˮ�е��ܽ�ȱ�ͬ������Ԫ�ص��⻯���ܶ��ԭ����____________________________________________________________________________________��
��5��������γɵľ�����۵���ڢ�����γɵľ�����۵㣬ԭ��____________________________��

��6��1183K���£�Ԫ�����ĵ���Ϊ�����������壨�����ṹ��ͼ1����1183K����ת��Ϊ�����������壨�����ṹ��ͼ2������ͼ2�У���һ��ԭ�Ӿ����������ȵ�ԭ�Ӹ���Ϊ________��ͼ1��ͼ2��ʾ�����к��е�ԭ�Ӹ���֮��Ϊ________��
���𰸡��� ![]() ��
��![]() sp ���Ӿ��� �� ��������ˮ����֮����γ�����ҷ�����ѧ��Ӧ
sp ���Ӿ��� �� ��������ˮ����֮����γ�����ҷ�����ѧ��Ӧ ![]() �İ뾶��
�İ뾶��![]() ��С��ʹ������þ����ľ����ܴ�����þ���� 12 1:2
��С��ʹ������þ����ľ����ܴ�����þ���� 12 1:2
��������
��Ԫ�������ڱ���λ�ÿ�֪����ΪBe����ΪC����ΪN����ΪO����ΪMg����ΪAl����ΪS����ΪCl����ΪFe����ΪCu��
��1��Ԫ�����ڱ���λ��ds����Ԫ��Ϊ�ڢ�B����B�壬�ʷ��ϵ�Ϊ��Ԫ��ͭ����Ԫ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ[Ar]3d104s1��
�ʴ�Ϊ�⣻[Ar]3d104s1��![]() ��
��
��2���ٺ͢��γɵĻ�����ΪBeCl2��Be�����¶�ԭ�ӣ��γ�2�����۵�����������ԭ�ӵ��ӻ��������Ϊsp�ӻ����͢��γɵĻ�����ΪAlCl3���ɷ��ӹ��ɣ�Ϊ���Ӿ��壬
�ʴ�Ϊsp�����Ӿ��壻
��3��Nԭ�ӵ�2p���Ӱ���Ϊ�ȶ��ṹ�����һ�����ܴڡ��ۡ�������Ԫ���У���һ�����������Ǣڣ�
�ʴ�Ϊ�ڣ�
��4��Ԫ�آ۵ļ���̬�⻯��Ϊ����������ˮ�����γ��������Ԫ�آ۵ļ���̬�⻯����ˮ�е��ܽ�ȱ�ͬ������Ԫ�ص��⻯���ö��ԭ���Ƿ���֮���γ������
�ʴ�Ϊ����֮���γ������
��5��������γɵľ��壨MgO�����۵���ڢ�����γɵľ��壨MgS���۵㣬ԭ��Ϊ�����Ӱ뾶С�������Ӱ뾶����MgO�����Ӽ��̣����ܴ�
�ʴ�Ϊ�����Ӱ뾶С�������Ӱ뾶����MgO�����Ӽ��̣����ܴ�
��6����ͼ1��֪��������ԭ�Ӿ��������ԭ��λ�ڶ��㣬����8������ͼ2��֪���붥��ԭ�Ӿ��������ԭ��λ�����ģ�1����������3�����ռ���8��������϶���ã���1���汻2���������ã�����һ��ԭ�Ӿ����������ȵ�ԭ�Ӹ���Ϊ![]() =12����ͼ1��ͼ2��ʾ�����к��е�ԭ�Ӹ���֮��Ϊ��1+8��
=12����ͼ1��ͼ2��ʾ�����к��е�ԭ�Ӹ���֮��Ϊ��1+8��![]() ������6��
������6��![]() +8��
+8��![]() ��=1��2��
��=1��2��
�ʴ�Ϊ12��1��2��


 ����ѧ���ʱѧ����ϵ�д�
����ѧ���ʱѧ����ϵ�д� �ʰ�Ӣ��ͬ����ϰ��ϵ�д�
�ʰ�Ӣ��ͬ����ϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij���淴Ӧ��mA(g)+nB(g)![]() xC(g) ����=Q kJmol-1�����ܱ������н��У���ʾ��Ӧ�ڲ�ͬʱ��t���¶�T��ѹǿP��C�ڻ�������еİٷֺ���(C%)�Ĺ�ϵ���ߣ��� ��
xC(g) ����=Q kJmol-1�����ܱ������н��У���ʾ��Ӧ�ڲ�ͬʱ��t���¶�T��ѹǿP��C�ڻ�������еİٷֺ���(C%)�Ĺ�ϵ���ߣ��� ��

A.T1>T2��P1>P2��m+n>x��Q>0B.T1<T2��P1<P2��m+n<x��Q>0
C.T1>T2��P1<P2��m+n<x��Q<0D.T1<T2��P1<P2��m+n>x��Q<0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������ӵ�أ������������¿ɽ���ѭ����ŵ磬ʵ�ֶԴ��ԵĿ�����ء�һ��Ϊ����Fe2O3����һ��Ϊ����﮺�ʯī�ĸ��ϲ��ϣ������ֻ��������ӡ�����ܷ�ӦΪ��Fe2O3+6Li![]() 2Fe+3Li2O�����ڴ˵�أ�����˵������ȷ����
2Fe+3Li2O�����ڴ˵�أ�����˵������ȷ����
A.�ŵ�ʱ���˵����������
B.�ŵ�ʱ��������ӦΪFe2O3+6Li++6e-= 2Fe+3Li2O
C.�ŵ�ʱ������������С��������������
D.���ʱ��������ӦΪLi++e-=Li
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�CH4��H2O(g)������Ӧ��CH4(g)+H2O(g)![]() CO(g)+3H2(g)������ʼ
CO(g)+3H2(g)������ʼ![]() =Z���ں�ѹ�£�ƽ��ʱ
=Z���ں�ѹ�£�ƽ��ʱ![]() (CH4)�����������Z��T���¶ȣ��Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
(CH4)�����������Z��T���¶ȣ��Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
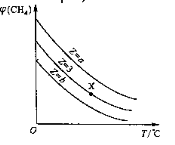
A���÷�Ӧ���ʱ䦤H��0
B��ͼ��Z�Ĵ�СΪb��3��a
C��ͼ��X���Ӧ��ƽ��������![]() =3
=3
D���¶Ȳ���ʱ��ͼ��X���Ӧ��ƽ���ڼ�ѹ��![]() (CH4)��С
(CH4)��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϻ����㷺Ӧ���ڶ������͵��㾫�У���ṹ��ʽ��ͼ��ʾ������˵������ȷ����( )
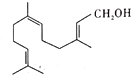
A.��ϻ�����ͬ���칹���в������з�������
B.��ϻ����ɷ����ӳɷ�Ӧ��ȡ����Ӧ��������Ӧ
C.��ϻ������ӵķ���ʽΪC15H26O
D.1 mol��ϻ���������Na��Ӧ����0.5 mal������������NaHCO3��Һ��Ӧ����1 mol CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���磭Fenton��������ˮ�����л���Ⱦ�オ��ĸ�������������Ӧԭ����ͼ��ʾ����������H2O2��Fe2+������Ӧ���ɵ��ǻ����ɻ�����OH�������������л���Ⱦ�����˵���������

A.��Դ��A��Ϊ����
B.���ԴB�������缫�ĵ缫��ӦʽΪH2O��e- ��H+����OH
C.Fenton��ӦΪ��H2O2��Fe2+��Fe(OH)2+����OH
D.ÿ����2.24LO2����״���������������������Ͽɲ�������OHΪ0.2mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ��![]()
![]()
��![]()
![]()
�ڲ�ͬ�¶�ʱ![]() ��
��![]() ��ֵ�����
��ֵ�����
�¶� |
|
|
973 |
|
|
1173 |
|
|
�ݴ˿�֪��Ӧ�ۣ���![]()
![]() ���������Ϣ��ȷ���ǣ� ��
���������Ϣ��ȷ���ǣ� ��
A.![]()
B.�÷�Ӧ����ӦΪ���ȷ�Ӧ
C.�÷�Ӧ����ʱ���Ϸ����![]() ���������
���������![]() ��ת���ʺͷ�Ӧ����
��ת���ʺͷ�Ӧ����
D.�ں������ݻ��ɱ�������з�����Ӧ�ۣ�ѹ�������Ӧ���ʻ�����![]() Ҳ����
Ҳ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)12g̼������ˮ������Ӧ����CO��H2��������131.3KJ�������˷�Ӧ���Ȼ�ѧ����ʽΪ______________________________��
(2)��֪���µ��Ȼ�ѧ��Ӧ����ʽ��
��2CO��g��+O2��g����2CO2��g�� ��H����566kJ/mol
��2H2��g��+O2��g����2H2O��g�� ��H����484kJ/mol
��CH4��g��+2O2��g����CO2��g��+2H2O��g�� ��H����890kJ/mol
��CH4��g��+CO2��g����2CO��g��+2H2��g�� ��H��______��
(3)��֪H2(g)+Br2(l)=2HBr(g) ��H=��102kJ/mol������������������±���
H2(g) | Br2(l) | HBr(g) | |
1mol�����еĻ�ѧ������ʱ��Ҫ���յ�����/kJ | 436 | a | 369 |
�����aΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����a��b������������������Һ��ζ��ĵζ����ߣ�����������ȷ����( )

A.P��ʱǡ����ȫ��Ӧ����Һ������
B.��������ʵ���Ũ��Ϊ1 mol��L��1
C.��̪����������ʵ���ָʾ��
D.����a������ζ�����������Һ�ĵζ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com