
【题目】实验室利用二氧化锰和浓盐酸反应制取Cl2,化学方程式如下:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)请用单线桥标出该反应电子转移的方向和数目__,该反应的氧化产物是__。
(2)其中氧化剂与还原剂的物质的量之比是__;若实验中有87g的MnO2完全反应,则制得的Cl2在标况下的体积是__L。
【答案】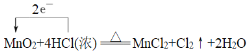 Cl2 1:2 22.4
Cl2 1:2 22.4
【解析】
反应中Mn元素化合价从+4价降低到+2价,Cl元素化合价从-1价升高到0价,结合电子得失守恒以及氧化还原反应的有关概念分析解答。
(1)反应MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O中Mn元素的化合价由+4降低为+2价,得到2个电子,Cl元素的化合价由-1升高为0价,失去1个电子,则根据电子得失守恒可知转移的电子数为2个,因此单线桥法标出该反应电子转移的方向和数目为
MnCl2+Cl2↑+2H2O中Mn元素的化合价由+4降低为+2价,得到2个电子,Cl元素的化合价由-1升高为0价,失去1个电子,则根据电子得失守恒可知转移的电子数为2个,因此单线桥法标出该反应电子转移的方向和数目为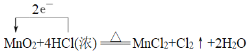 ,其中该反应的氧化产物是Cl2;
,其中该反应的氧化产物是Cl2;
(2)根据电子得失守恒可知氧化剂与还原剂的物质的量之比是1:2;若实验中有87g的MnO2完全反应,二氧化锰的物质的量是1mol,则制得的Cl2是1mol,在标况下的体积是22.4L。


科目:高中化学 来源: 题型:
【题目】研究CO2的综合利用对促进“低碳经济”的发展有重要意义。
(1)工业上以CO2、NH3为原料生产尿素[CO(NH2)2],反应实际为两步进行:
I:2NH3(g)+CO2(g)![]() H2NCOONH4(s) △H1=-272kJ·mol-1
H2NCOONH4(s) △H1=-272kJ·mol-1
II:H2NCOONH4(s)![]() CO(NH2)2(s)+H2O(g) △H2=+138kJ·mol-1
CO(NH2)2(s)+H2O(g) △H2=+138kJ·mol-1
已知:H2O(l)==H2O(g) △H3=+44kJ·mol-1
①请写出以NH3、CO2为原料,合成尿素和液态水的热化学方程式______________。
②T1℃时,在1L的密闭容器中充入CO2和NH3模拟工业生产,n(NH3)/n(CO2)=x,如图是CO2平衡转化率(![]() )与x的关系。求图中A点NH3的平衡转化率
)与x的关系。求图中A点NH3的平衡转化率![]() =________%。
=________%。
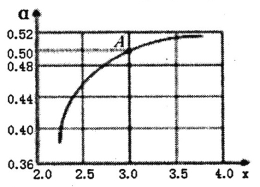
③当x=1.0时,若起始的压强为p0kPa,水为液态,平衡时压强变为起始的1/2。则该反应的平衡常数Kp=_______(kPa)-3(KP为以分压表示的平衡常数)。
(2)用CO2和H2合成甲醇:3H2(g)+CO2(g)![]() CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。在T℃时,甲、乙、丙三个2L的恒容密闭容器中,按不同方式投入反应物,测得平衡时有关数据如下:
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。在T℃时,甲、乙、丙三个2L的恒容密闭容器中,按不同方式投入反应物,测得平衡时有关数据如下:
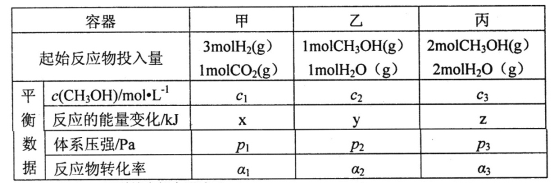
①甲容器10s达到平衡时测得x=39.2,则甲中CO2的平均反应速率____________。
②下列说法正确的是________(填字母编号)。
A.2c1<c3 B.z<2y C.p3>2p2 D.α1+α3>1
(3)用NaOH溶液做碳捕捉剂可获得化工产品Na2CO3。常温下若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=_____[K1(H2CO3)=4.4×10-7、K2(H2CO3)=5×10-11],溶液中c(Na+)_____c(HCO3-)+2c(CO32-)(填“>”“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关蛋白质的叙述不正确的是![]()
![]()
![]() 向蛋白质溶液里加
向蛋白质溶液里加![]() 溶液可提纯蛋白质
溶液可提纯蛋白质
![]() 蛋白质的分子能透过半透膜
蛋白质的分子能透过半透膜
![]() 蛋白质水解的最终产物是氨基酸
蛋白质水解的最终产物是氨基酸
![]() 温度越高,酶对某些化学反应的催化效率越高
温度越高,酶对某些化学反应的催化效率越高
![]() 任何结构的蛋白质遇到浓
任何结构的蛋白质遇到浓![]() 都会变黄色
都会变黄色
A.①②③B.②③⑤C.③④⑤D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A.有氧气参与的反应都是放热反应
B.热化学方程式既表示能量的变化,又表示物质的变化
C.若2CO2(g)![]() 2CO(g)+O2(g)△H=+566kJ·mol-1,则CO的燃烧热△H=-566 kJ·mol-1
2CO(g)+O2(g)△H=+566kJ·mol-1,则CO的燃烧热△H=-566 kJ·mol-1
D.放热反应理论上都可以设计为原电池,将化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在有、无催化剂时,HI分解反应的能量随反应进程的变化关系如图所示,下列说法正确的是
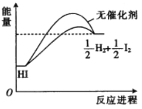
A.其他条件不变时,升高温度,平衡体系中HI的含量降低
B.图示中无催化剂的反应焓变更高
C.其他条件不变时,增大压强,可提高HI的平衡转化率
D.催化剂可提高分子的能量,加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸广泛应用在稀有金属的湿法冶金、漂染工业、金属加工、无机药品及有机药物的生产等领域中。HCl极易溶于水,工业上用HCl气体溶于水的方法制取盐酸。
(1)用密度为1.2g/mL,质量分数为36.5%的浓盐酸配制250mL3mol/L的稀盐酸,需要用量筒量取浓盐酸的体积为__mL。
(2)溶液配制中需要的玻璃仪器有烧杯、玻璃棒、量筒、__、__。
(3)实验过程中,下列操作会导致最终所配溶液浓度偏高的是__。
A.量取浓盐酸时俯视刻度线
B.实验前,容量瓶中有少量残留蒸馏水
C.定容时俯视刻度线
D.转移时,未洗涤烧杯和玻璃棒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳;②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物;③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物;④将得到的产物熔融电解得到镁。下列说法不正确的是
A. 此法的优点之一是原料来源丰富
B. ①②③步骤的目的是从海水中获取MgCl2
C. 第④步电解得到,镁的方程式为MgCl2(熔融)![]() Mg+Cl2↑
Mg+Cl2↑
D. 提取镁的过程涉及化合、分解、置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
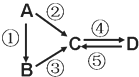
(1)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出②反应的离子方程式_________;④反应离子方程式__________。
(2)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种黄绿色气体单质。写出A与水高温下反应的化学方程式_______________________。④反应的离子方程式______________。D中加入氢氧化钠的现象__________。
(3)若A是太阳能电池用的光伏材料,B常用用于制作高档光学器材,C、D为钠盐,C的水溶液俗称泡花碱,D的溶液显碱性。④反应也是通入一种引起温室效应的主要气体。写出③反应的化学方程式________________________。⑤反应用到B,反应条件为高温,则⑤的化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知非金属元素A、B、C、D、E均属于短周期元素,其原子序数依次增大,A元素原子形成的离子核外电子数为零,B原子的最外层电子数是内层电子数的2倍,通常状况下E的单质是黄色晶体,不溶于水,易溶于二硫化碳,D与E在同一主族,C、D在周期表中处于相邻的位置,请回答下列问题:
(1)B元素的名称是___,E的阴离子结构示意图是___。
(2)A元素与元素周期表中非金属性最强的元素形成化合物M,M溶液常被用来刻蚀玻璃,刻蚀玻璃的化学方程式为____。
(3)元素C的最高价氧化物对应水化物与其气态氢化物反应生成化合物Z,该反应的离子方程式为____,形成化合物Z的阳离子在实验室中如何检验?简述操作步骤。____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com