
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、自然界中含有大量的游离态的硅,纯净的硅晶体可用于制作计算机芯片 | B、金属铝、铁、铜都有一定的抗腐蚀性能,其抗腐蚀的原因都是表而形成氧化物薄膜,阻止反应的进一步进行 | C、工业上通常用电解钠、铁、铜对应的氯化物制得该三种金属单质 | D、Si、P、S、Cl相应的最高价氧化物对应水化物的酸性依次增强 |
查看答案和解析>>
科目:高中化学 来源:浙江省模拟题 题型:填空题
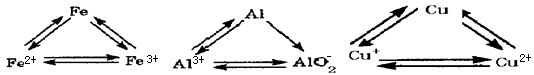




查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com