
分析 (1)氯水中氯气与KI发生氧化还原反应生成碘和KCl;
(2)强电解质能完全电离;
(3)铁丝在氯气中燃烧产生氯化铁;
(4)氟单质通人氯化钠溶液中,会和水之间反应产生氧气.
解答 解:(1)氯水中氯气与KI发生氧化还原反应生成碘和KCl,溶液变黄,反应为2KI+Cl2=I2 +2KCl,故答案为:2KI+Cl2=I2 +2KCl;
(2)碳酸氢钠属于盐,能完全电离,即:NaHCO3=Na++HCO3-,故答案为:NaHCO3=Na++HCO3-;
(3)铁丝在氯气中燃烧出现黄棕色的烟,即产生氯化铁,反应为:3Cl2+2Fe$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,故答案为:3Cl2+2Fe$\frac{\underline{\;点燃\;}}{\;}$2FeCl3;
(4)氟单质通人氯化钠溶液中,会和水之间反应产生氧气,即2F2+2H2O=4HF+O2↑,故答案为:2F2+2H2O=4HF+O2↑.
点评 本题考查学生方程式的书写知识,注意物质的性质是关键,难度不大.


科目:高中化学 来源: 题型:解答题
 生物质资源是一种污染小的可再生能源,可由其制得多种化工原料,如甲醛、甲醇和二甲醚等.
生物质资源是一种污染小的可再生能源,可由其制得多种化工原料,如甲醛、甲醇和二甲醚等.| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molCO、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH平衡时浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 平衡常数 | K1 | K2 | K3 |
| 反应物转化率 | a1 | a2 | a3 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
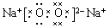
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气和氯气反应生成氯化氢气体是放热反应,所以不需要条件就能自发进行 | |
| B. | 氢气和氯气反应生成2 mol氯化氢气体,反应吸收183 kJ的热量 | |
| C. | 氢气和氯气反应生成2 mol氯化氢气体,反应放出183 kJ的热量 | |
| D. | 氢气和氯气反应生成1 mol氯化氢气体,反应放出183 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| n(CO2)(mol) | 6 | 4 | 3 | 2 |
| n(沉淀)(mol) | 2 | 3 | 2 | 1 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期第IA族 | B. | 第四周期第IA族 | C. | 第五周期第IA族 | D. | 第二周期第IIA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁原子的电子排布式:[Ar]3d64s2 | B. | 核内有8个中子的碳原子:${\;}_{6}^{8}$C | ||
| C. | 氢氧化钠的电子式: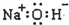 | D. | F的原子结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体粒子能够发生布朗运动 | B. | 胶体粒子带电荷 | ||
| C. | 胶体粒子直径在1-100nm之间 | D. | 胶体粒子不能穿过半透膜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com