
分析 A、B、C、D分别是AlCl3、BaCl2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下:
①C+D→白色沉淀,加入稀硝酸,沉淀不溶解,说明该沉淀是BaSO4沉淀;
②B+D→白色沉淀,在空气中放置,沉淀由白色迅速变为灰绿色,最后转化为红褐色,则该白色沉淀是Fe(OH)2,结合①知,D是FeSO4、B是NaOH、C是BaCl2,
③A+B→白色沉淀,继续加入B溶液,白色沉淀逐渐消失,A是AlCl3,
结合题目分析解答.
解答 解:A、B、C、D分别是AlCl3、BaCl2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下:
①C+D→白色沉淀,加入稀硝酸,沉淀不溶解,说明该沉淀是BaSO4沉淀;
②B+D→白色沉淀,在空气中放置,沉淀由白色迅速变为灰绿色,最后转化为红褐色,则该白色沉淀是Fe(OH)2,结合①知,D是FeSO4、B是NaOH、C是BaCl2,
③A+B→白色沉淀,继续加入B溶液,白色沉淀逐渐消失,A是AlCl3,
(1)通过以上分析知,A、B、C、D分别是AlCl3、NaOH、BaCl2、FeSO4,故答案为:AlCl3;NaOH;BaCl2;FeSO4;
(2)①实验②中沉淀由白色迅速变为灰绿色,最后转化为红褐色,先生成氢氧化亚铁沉淀,氢氧化亚铁不稳定,易被氧化生成红褐色沉淀氢氧化铁,该反应的化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
②A溶液与B溶液反应后生成的白色沉淀溶解于B溶液中的离子方程式 Al(OH)3+OH-=AlO2-+H2O,故答案为:Al(OH)3+OH-=AlO2-+H2O;
③C与D反应的离子方程式Ba2++SO42-=BaSO4↓,故答案为:Ba2++SO42-=BaSO4↓.
点评 本题考查无机物的推断,题目难度不大,注意根据物质的性质以及反应的现象判断可能发生的反应,以此确定物质的种类,把握物质反应的化学方程式、离子方程式是解答该题的关键.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
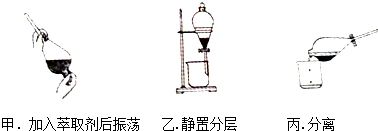 某同学采用萃取-分液的方法从碘水中提取碘,主要操作步骤如图:
某同学采用萃取-分液的方法从碘水中提取碘,主要操作步骤如图:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
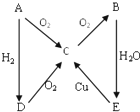 如图A→E是五种中学化学常见物质其中A、B、C、D常温下都是气体,B 为红棕色,A为气体单质.
如图A→E是五种中学化学常见物质其中A、B、C、D常温下都是气体,B 为红棕色,A为气体单质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水玻璃中通入少量二氧化碳:Na2SiO3+CO2+H2O═2Na++CO32-+H2SiO3 | |
| B. | 饱和石灰水中通入过量二氧化碳:Ca(OH)2+2CO2═Ca2++2HCO3- | |
| C. | 向KI溶液中滴入稀硫酸,并且在空气中充分振荡:4H++4I-+O2═2I2+2H2O | |
| D. | 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡含有食品添加剂的食物对人体健康均有害,不宜食用 | |
| B. | 不慎误服BaCl2溶液时,除大量吞服鸡蛋清解毒外,还应加服一定量的解毒剂碳酸钠,以便将BaCl2转化成碳酸钡 | |
| C. | 某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2 | |
| D. | 食盐可作调味剂,也可作食品防腐剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com