
| A.+6 |
| B.+3 |
| C.+2 |
| D.0 |
科目:高中化学 来源:不详 题型:填空题
| A.酸性 | B.氧化性 | C.吸水性 | D.脱水性 |
 物质的量是 mol。
物质的量是 mol。查看答案和解析>>
科目:高中化学 来源:不详 题型:判断题
 )。
)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.+6 |
| B.+4 |
| C.+2 |
| D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②③ | C.③④ | D.①④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ①
①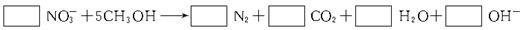
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NF3是氧化剂,H2O是还原剂 |
| B.还原剂与氧化剂的物质的量之比为2:1 |
| C.若生成0.2 mol HNO3,则转移0.2 mol电子 |
| D.NF3在潮湿的空气中泄漏会产生红棕色气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com