
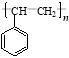
����Ŀ����Ȳ��һ����Ҫ���л�����ԭ�ϣ�����ȲΪԭ���ڲ�ͬ�ķ�Ӧ�����¿���ת�������»����������и��⣺

��1������������Ķ���ȡ��������________�֡�
��2��������ϩ����Ȳ���ӵ�˵����ȷ����________��
A����ʹ����KMnO4��Һ��ɫ
B��1Ħ����ϩ����Ȳ����3Ħ��Br2�����ӳɷ�Ӧ
C����ϩ����Ȳ�����ں������ֹ�����
D������������Ȳ����ϩ����Ȳ��ȫȼ��ʱ�ĺ���������ͬ
��3��д���뻷����ϩ��Ϊͬ���칹�������ڷ������ķ��ӷ����Ӿ۷�Ӧ�Ļ�ѧ����ʽ
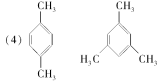
��4��д���뱽��Ϊͬϵ����һ��ȡ������ֻ�����ֵ����ʵĽṹ��ʽ(������)��__________________��__________________��
���𰸡���1��1
��2��ABC
��3��n![]() ��
�� ��
��
��������
�����������1�� ���������飬������Գ��Կ�֪�����ȴ���ֻ��1�֡���
��2����ϩ����Ȳ����̼̼˫����̼̼������������ʹ����KMnO4��Һ��ɫ��1Ħ����ϩ����Ȳ����3Ħ��Br2�����ӳɷ�Ӧ����ϩ����Ȳ���Ӻ���̼̼˫����̼̼�������ֹ���������Ȳ����ϩ����Ȳ���ʽ��ͬ������������Ȳ����ϩ����Ȳ��ȫȼ��ʱ�ĺ�������ͬ��
��3��������ϩ����ʽΪC8H8���ȱ�������C8H18��10��H��һ��������8��H�����Ի�����ϩ�����ڷ�������ͬ���칹��ṹ�г�����һ�������⣬��Ӧ����һ��C==C�������Ӿ۷�Ӧ�Ļ�ѧ����ʽn![]() ��
��![]() ��
��
��4��һ�ȴ���ֻ�����ֱ���ͬϵ��ڽṹ��Ӧ���нϺõĶԳ��ԣ��ȴ�ʱ������ȡ�������ϵ��⣬Ҳ����ȡ�������ϵ��⣬
 ��
��


 ������ϵ�д�
������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ũ������Ҵ���ȡ��ϩʱ�����ῴ����ƿ��Һ���ڣ��Ƶõ���ϩ�л���CO2��SO2�����ʡ�ij����С�����������װ�ã�֤����ϩ�л���CO2��SO2����֤��ϩ�����ʡ�
�ش��������⣺

��1��װ��A����ϩ�ķ���װ�á�ͼ��һ�����ԵĴ�����__________����ƿ�����Ƭ��������__________��
��2����Ҫ����A���������庬��SO2���ɽ���Ϻ�����ֱ��ͨ��__________������ţ���ͬ��װ�ã���Ҫ���飬A���������庬��CH2=CH2���ɽ����������ͨ��Bװ�ã�Ȼ��ͨ��__________װ�á�
��3��д��ʵ������ȡ��ϩ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I. �������顱��һ���˹��ϳɵ����������Ϊ������ṹ����̼�ܽṹ��ͼ��ʾ��
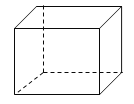
��1���������顱�ж���ͬ���칹�壬����һ�����ڷ�������ͬ���칹��Ľṹ��ʽ�� ��
��2�������顱�����ȴ������ͬ���칹�����Ŀ�� ��
II���л���ѧ�еķ�Ӧ���ͽ϶࣬�����з�Ӧ���ࣨ����ţ���
�������ڿ�����ȼ�� ������Ȳ������ϩ
�ۼ����������ڹ��յ������·�Ӧ ����ϩʹ���Ը��������Һ��ɫ
����ϩʹ������Ȼ�̼��Һ��ɫ ��ʵ��������ϩ
���ɼױ���ȡTNT ����������������Ƶ��Ҵ���Һ����
���ұ����Ʊ���![]()
��1����������ȡ����Ӧ����__________������������Ӧ����_______��
��2��д���ߺ͢�Ļ�ѧ����ʽ��
��_______________________ _____________________________
��_______________________ _____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��3��5-����������������Ҫ���л��ϳ��м��壬��������Ȼ���ʰ������صĺϳɡ�һ���Լ䱽����Ϊԭ�ϵĺϳɷ�Ӧ���£�

�״������Ѻ�3��5-�����������ӵIJ����������ʼ��±���
���� | �е�/�� | �۵�/�� | �ܶ�(20��) / g��cm-3 | �ܽ��� |
�״� | 64. 7 |
| 0. 7915 | ������ˮ |
���� | 34. 5 |
| 0. 7138 | ����ˮ |
3��5-������������ |
| 33-36 |
| �����ڼ״������ѣ�����ˮ |
��Ӧ�������ȷ�����״����ټ������ѽ�����ȡ��
��1���ٷ�����״��IJ����ǵ� ��
����ȡ�õ��ķ�Һ©��ʹ��ǰ�� ��ϴ������Һʱ�л����ڷ�Һ©���� ����ϡ����¡����㡣
��2������õ����л��������ñ���NaHCO3��Һ������ʳ��ˮ����������ˮ����ϴ�ӡ��ñ���NaHCO3 ��Һϴ�ӵ�Ŀ���� ���ñ���ʳ��ˮϴ�ӵ�Ŀ���� ��
��3��ϴ����ɺ�ͨ�����²������롢�ᴿ�����ȷ�IJ���˳���� (����ĸ)��
a�������ȥ���� b���ؽᾧ c�����˳�ȥ����� d��������ˮCaCl2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�������������ܱ������еķ�Ӧ��
N(g)+3H2(g)![]() 2NH3(g)����20����30MPa��n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ������������ȷ���ǣ���
2NH3(g)����20����30MPa��n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ������������ȷ���ǣ���

A����a������Ӧ���ʱ�b ��С
B����c����Ӧ�ﵽƽ��
C����d(t2ʱ�̣��͵�e(t2ʱ�̣���n(N2����һ��
D�������������䣬�÷�Ӧ��25���·�Ӧ�ﵽƽ��״̬�����õ�ʱ���ԭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ������ᶡ���¹�����һ�ֵ���ɫ����״Һ�壬�ܶ�Լ0.97g/cm3��������������ϩ����֬�����ܼ�����ҵ������ԭ�������������£�
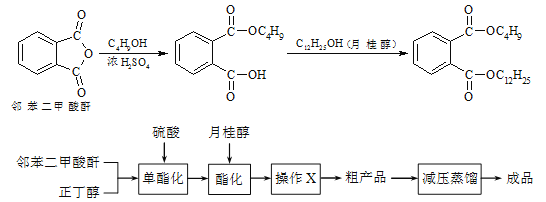
�й����ʵ��������ʼ��±���
������ | �ܽ��� | �۵� | �е� |
�ڱ��������� | ������ˮ�����ѣ��������ȱ����Ҵ������� | 131.6�� | 295�� |
������ | ����ˮ�������Ҵ����ѡ������л��ܼ� | -88.9�� | 117.5�� |
�¹� | ������ˮ�����ڴ����� | 24 | 259�� |
�ڱ������ᶡ���¹��� | ������ˮ�����ڶ����л��ܼ� | ���� | 202��210�� |
ijʵ��С���ͬѧģ�ҵ�����Ĺ������̣�����ͼ��ʾװ����ȡ�����ڱ������ᶡ���¹�����ͼ�мгֺͼ���װ������ȥ����Ҫ�����������£�
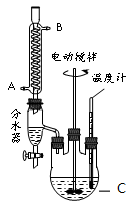
����������ƿ�ڼ���30 g �ڱ�����������16 g �������Լ�����Ũ���ᡣ
�����裬������105 �����������跴Ӧ1Сʱ��
����ȴ�����£�����40 g �¹�������160 �������衢��������Ӧ������
����ȴ�����£�����Ӧ����ﵹ����
��ͨ�����������еIJ���X���õ��ֲ�Ʒ��
��ش��������⣺
��1������C������___________������������ˮӦ��___________����
��2����������жϷ�Ӧ�ѽ����ķ�����___________��
��3��������в���X�ɳ�ȥ����δ��Ӧ���ڱ�����������������������X����___________��
��4�����������м�ѹ�����Ŀ����___________��
��5��ʵ������������ڡ��۲��ʶ��Ƚϸߣ�ԭ����___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��ش�����������
��1������������������70��ʱ��Ӧ����������NaClO3��NaClO�����ʵ���֮��Ϊ3�U1�����ӷ���
ʽ
��2����SO2ͨ������Fe(NO3) 3ϡ��Һ�У���Һ����ɫ��Ϊdz��ɫ�������ŷ�Ӧ�Ľ���������Һ�����ֱ�Ϊ�ػ�ɫ��Һ��������ɫ����������Թܿ�Ϊ����ɫ�ڵ����ӷ���ʽ ��
��3��2K37ClO3+4H35Cl��2KCl+2ClO2�� +Cl2�� +2H2O�ڸ����������ɵ�������Ħ������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��ú�DZ���Ļ�ʯȼ�ϣ����ǽ�úֱ����Ϊȼ��̫�˷ѣ�����ͨ��ú��______��ý�̿��ú���ͺͳ�¯ú���Ȳ�Ʒ��ú��������ָ��ú�ڸ�������ˮ�Ӵ�ת��Ϊ����Ϊ��ҵ������ȼ���Լ������ϳ�ԭ�ϵ�ú������д��ú�������Ļ�ѧ��Ӧ����ʽ:_________________��
��2����A1��Fe2O3��ɵ����ȼ���ַ�Ӧ��Ĺ���ֳ����ȷݣ�һ����������NaOH��Һ��Ӧ���ɱ����6.72�������壬��һ����������HCl��Һ��Ӧ���ɱ����17.92���������������ȷ�Ӧ�ķ���ʽΪ____________________��ԭ���ȼ�����Ϊ______�ˡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��A��J�ֱ������ط�Ӧ��һ�����ʡ���֪A�ֽ�õ������ʵ�����B��C��D��ͼ���в���������δ���������д���¿հף�

��1��A�к��еĻ�ѧ����________��
��2��д��ͭ��J��Ӧ��ȡH�Ļ�ѧ����ʽ��__________________________________________��
��3��д����Ӧ�������ӷ���ʽ��_________________________________________��
��4��д������B�ĵ���ʽ��_______________��д������E�ĵ���ʽ��_______________��
��5���ڷ�Ӧ���У������ɱ����22.4 L ����Gʱ��ת�Ƶ�����Ϊ________mol��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com