
下列各图中的大黑点代表原子序数从1~18号元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表共价键。下列各图表示的结构与化学式一定不相符的是( )
| A | B | C | D |
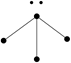 |  | 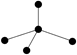 |  |
| NH3 | C2H2 | CCl4 | CO2 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:单选题
韩国首尔大学的科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”。则关于“暖冰”的判断正确的是
| A.“暖冰”中存在离子键 |
| B.“暖冰”中水分子的O-H键是非极性键 |
| C.“暖冰”的密度大,有导电性和导热性 |
| D.水凝固形成20℃时的“暖冰”所发生的变化是物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为( )
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 |
| C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强 |
| D.以上说法都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知CO2、BF3、CH4、SO3都是非极性分子,NH3、H2S、H2O、SO2都是极性分子,由此可推知ABn型分子是非极性分子的经验规律是( )
| A.分子中所有原子在同一平面内 |
| B.分子中不含氢原子 |
| C.在ABn分子中,A元素为最高正价 |
| D.在ABn型分子中,A原子最外层电子都已成键 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
| A.N2、CS2、H2O、CH4都是非极性分子 |
| B.SiO2、CsCl、HCl、HF四种晶体的熔点逐渐降低 |
| C.CO2、PCl3、CCl4、CH4四种分子中,各原子都满足最外层8电子结构 |
| D.由原子序数为1和8、1和6的元素,可分别形成原子数之比为1:1的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
H2S分子中两个共价键的夹角接近90°,其原因是( )。
| A.共价键的饱和性 |
| B.S原子电子排布 |
| C.共价键的方向性 |
| D.S原子中p轨道的形状和空间伸展方向 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com