
X、Y、Z、R、W是5种短周期元素,原子序数依次增大,它们可组成离子化合物Z2Y和共价化合RY3、XW4,已知Y、R同主族,Z、R、W同周期。下列说法不正确的是
| A.原子半径 :Z>R>W |
| B.X2W6分子中各原子均满足8电子结构 |
| C.气态氢化物的稳定性:HmW>HmR |
| D.Y、Z形成的化合物中只可能存在离子键 |
D
解析试题分析:根据题意可推出:X是C;Y是O;Z是Na;R是S;W是Cl。A.Na、S、Cl是同一周期的元素,随着原子序数的增大,原子半径逐渐减小。所以原子半径:Na>S>Cl。正确。B.C2Cl6中每个C与3个Cl形成三对共用电子对,和另一个C形成一对共用电子对。每个Cl与C形成一对共用电子对。所以每个原子都满足最外层8电子的稳定结构。正确。C.元素的非金属性:Cl>S。元素的非金属性越强,其对应的氢化物就越稳定。所以稳定性HCl>H2S。正确。D.Y、Z形成的化合物可以是Na2O、Na2O2。在Na2O中只存在离子键,在Na2O2既存在离子键,也存在非极性共价键。错误。
考点:考查元素的推断及元素的原子半径、氢化物、分子中的原子结构及结合方式的比较的知识。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:单选题
四种短周期元素A、B、C、D在元素周期表中的相对位置如图所示,其中D形成的两种氧化物都是大气污染物。下列有关判断正确的是 ( )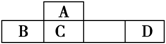
A.简单氢化物的热稳定性:C>A
B.最高价氧化物对应水化物的酸性:D<C
C.B的最高价氧化物的水化物能与D的最高价氧化物的水化物反应
D.A、C、D的最高价含氧酸的钠盐水溶液可能均显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.中国是目前全球最大的稀土提炼和加工国,对稀土元素及其化合物的研究是获得优良催化剂的一种重要途径 |
| B.气化、液化和干馏是煤综合利用的主要方法,这三者中只有干馏是化学变化 |
| C.原子核外在离核较远区域的电子易失去,其原因是这些电子能量较低 |
| D.醋酸纤维、硝化纤维、合成纤维、光导纤维都可由纤维素在一定条件下制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素W、X、Y、Z的原子序数依次增大,W、X原子的最外电子层电子数之比为4︰3,Z原子比X原子的核外电子数多4。下列说法正确的是
| A.W、Y、Z的电负性大小顺序一定是Z>Y>W |
| B.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z |
| C.Y、Z形成的分子的空间构型可能是正四面体 |
| D.WY2分子中σ键与π键的数目之比是2︰1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是
A 元素原子的最外层电子数等于元素的最高化合价
B 多电子原子中,在离核较近的区域内运动的电子能量较高
C P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强
D 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
目前人类已发现的非金属元素除稀有气体外共有16种,对这16种非金属元素的相关判断( )
①都是主族元素,最外层电子数都大于4
②单质在反应中都只能作氧化剂
③氢化物常温下都是气态,所以又叫作气态氢化物
④氧化物常温下都可以与水反应生成酸
⑤根据非金属原子最外层的电子数,可判断两种元素得电子能力的强弱
⑥非金属得电子后形成的简单阴离子的核外电子排布一定与上一周期稀有气体原子的核外电子排布相同
| A.④⑤正确 | B.①③⑥正确 |
| C.②③⑤正确 | D.都错误 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是
| 元素 代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | -1 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
A.P和S属于第三周期元素,P原子半径比S小
B.同周期ⅡA和ⅢA族元素的原子序数都相差1
C.短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则原子序数、原子半径和单质的还原性都按照A、B、C、D的顺序减小
D.Cl和Br属于第ⅦA族元素,HClO4酸性比HBrO4强。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com