
【题目】下列有关说法中正确的是
A.NH3与HCl气体或CO2气体均不能共存
B.铵盐溶液与NaOH溶液混合后会有NH3逸出
C.硅、二氧化硅、硅酸、铵盐受热均很稳定
D.SiO2能溶解在NaOH溶液但不能溶解在氨水中
科目:高中化学 来源: 题型:
【题目】有pH=2的盐酸溶液100mL,要使它的pH升为3.
(1)若加入蒸馏水,应加mL(不考虑溶液体积变化,下同).
(2)若加入pH为4的盐酸溶液,应加mL.
(3)若加入0.001molL﹣1的氢氧化钠,应加mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是( )
A. Na+、Al3+、Cl-、SO42-B. Mg2+、Cl-、NO3-、OH-
C. Ba2+、Na+、CO32-、NO3-D. H+、SO42-、NO3-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ||||||||
2 | B | C | D | E | ||||
3 | A | F | J | G | I |
(1)表中元素,化学性质最不活泼的是_______,最高价氧化物的水化物酸性最强的是__________
(2)B、C、D、E、G形成的气态氢化物中,最稳定的是________________
(3)A元素的最高价氧化物的水化物中所含化学键类型_________________,D元素的简单气态氢化物的电子式为_________,J的某原子中含有15个中子,试用恰当符号表示出该原子________
(4)E、F、G形成的简单离子半径由大到小的顺序________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下对于某些离子的检验及结论一定正确的是( )
A.将铜丝用盐酸洗涤后,蘸取NaCl溶液,在酒精灯上灼烧,观察焰色为黄色,证明含Na+
B.加入NaOH溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,原溶液中一定有NH4+
C.加入硝酸酸化的硝酸钡溶液产生白色沉淀,则一定有SO42-
D.加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中有关物质的浓度关系正确的是( )
A.1.0 mol/L Na2C2O4溶液中:c(OH﹣)═c(H+)+c(HC2O ![]() )+2c(H2C2O4)
)+2c(H2C2O4)
B.含等物质的量的NaHCO3和Na2CO3的溶液中:3c(Na+)=2[c(HCO ![]() )+c(CO
)+c(CO ![]() )+c(H2CO3)]
)+c(H2CO3)]
C.二元酸H2A在水中发生电离:H2A=H++HA﹣和HA﹣?H++A2﹣ , 则NaHA溶液中:c(Na+)>c(HA﹣)>c(OH﹣)>c(H+)
D.含有AgCl和AgI固体的悬浊液:c(Cl﹣)<c(I﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以干海带为原料提取碘单质和氯化钾的过程主要分三步:完成下列填空:
(1)步骤一:灼烧干海带,使其灰化后用热水浸泡、过滤,制得原料液,含有氯化钾等物质.实验室灼烧海带应放在(填写仪器名称)中加热,选用热水而不是冷水浸泡海带灰的目的是 .
(2)步骤二:原料液经结晶过滤分离出氯化钾后,向滤液中通适量氯气氧化I﹣ , 制得富碘溶液.实验室模拟氧化过程的实验装置如图所示.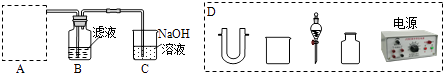
装置中A部分用于制取氯气,实验室制取氯气通常有两种方案:一是在强酸性条件下用氧化剂氧化Cl﹣;二是电解法.限用图D中的仪器(支撑仪器、导管、导线、石墨棒和橡皮塞除外),能实现的反应是(选填编号).
a.2NaCl(s)+MnO2+2H2SO4(浓) ![]() MnSO4+Cl2↑+Na2SO4+2H2O
MnSO4+Cl2↑+Na2SO4+2H2O
b.2KMnO4+16HCl(浓)→2MnCl2+2KCl+5Cl2↑+8H2O
c.2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
d.4HCl(浓)+MnO2 ![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
广口瓶B中发生反应的离子方程式是 . 装置C中NaOH的作用是 .
(3)步骤三:取100mL B中富碘溶液,按如下流程分离碘单质.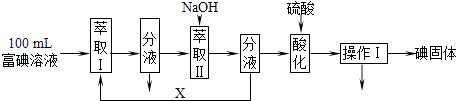
萃取Ⅱ和酸化过程发生的反应分别是:
3I2+6OH﹣→5I﹣+IO3﹣+3H2O;
5I﹣+IO3﹣+6H+→3I2+3H2O;
萃取剂X应选择(选填编号).
a.100mL苯b.10mL乙醇c.10mLCCl4d.10mL己烯
实验室进行萃取操作的仪器是 . 操作Ⅰ的名称是 .
(4)分离出的KCl样品中常含有少量NaCl和K2CO3等物质,设计实验用沉淀法测定氯化钾样品中K2CO3的质量分数:①要用到的化学试剂是(填写化学式);
②要测定的物理量是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,101kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5kJ/mol、285.8kJ/mol、890.3kJ/mol、2800kJ/mol,则下列热化学方程式正确的是( )
A.C(s)+ ![]() O2(g)=CO(g);△H=﹣393.5 kJ/mol
O2(g)=CO(g);△H=﹣393.5 kJ/mol
B.2H2(g)+O2(g)=2H2O(g);△H=+571.6 kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=﹣890.3 kJ
D.![]() C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=﹣1400 kJ/mol
C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=﹣1400 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com