
�Ȼ�ͭ���壨CuCl2��2H2O���к���FeCl2���ʣ�Ϊ�Ƶô������Ȼ�ͭ���壬���Ƚ����Ƴ�ˮ��Һ���ٰ���ͼ��ʾ�IJ�����������ᴿ��

������±�������������ա�
|
|
�������↑ʼ����ʱ��pH |
�������������ȫʱ��pH |
|
Cu2�� |
4.7 |
6.7 |
|
Fe2�� |
7.0 |
9.0 |
|
Fe3�� |
1.9 |
3.2 |
�Ų���I����X��Ŀ����___________________________ ��
���������ʶ�������ΪX���ʺϱ�ʵ���X���ʿ����ǣ���ѡ�_________ ��
A��KMnO4 B��H2O2 C��NaClO D��Cl2
�Dz���II��Y�Լ�Ϊ_______________���ѧʽ������������Һ��pH��______��Χ��
��ʵ����������CuCl2��Һʱ�������������������ǣ��������������й����ӷ���ʽ��ʾ��__________________________________________________________��
������CuCl2��Һ�������գ��õ��Ĺ�����_________________���ѧʽ������Ҫ����ˮCuCl2���������������______________________________________________��
����14�֣��ż�����������ʹFe2������ΪFe3����2�֣� ��B��D��2�֣�
��CuO��2�֣���3.2��pH��4.7��2�֣�
��Cu2��ˮ�⣺Cu2��+2H2O Cu(OH)2+2H�� ����2�֣���������������ˮ�⣨1�֣���
Cu(OH)2+2H�� ����2�֣���������������ˮ�⣨1�֣���
��CuO��2�֣���HCl������������1�֣���
��������
�������������Fe2+����ΪFe(OH)2��pHֵ��Cu2+����ΪCu(OH)2��pH�ϴ���Fe3+����ΪFe(OH)3��pH���ϴ����Կ���ͨ���Ƚ�Fe2+����ΪFe3+���ٵ�����Һ��pHʹ����Fe(OH)3������ʽ������ȥ��Ϊ��ʹ������������������µ����ʣ���Ȼ��H2O2��á�����ͬ���Ŀ��ǣ�����y������ҺpHֵʱ��Ӧѡ������H+��Ӧ�����ܽ�Ƚ�С��������CuOΪ�ã�CuO�Զ�����������Ҳ����ʹpHֵ����̫���ʹCu2+������
��1�����ݲ���I�����ӵı仯��֪������Ŀ���Ǽ����������������������������������ӵġ�
��2��������ʵ���в����������µ����ʣ�����ѡ��AC����ȷ��˫��ˮ�Ļ�ԭ������ˮ�������Ļ�ԭ�����������ӣ������������ʣ���ѡBD��
��3��Y�Լ���Ŀ���dz��������ӣ����Լ�����Լ�Ӧ��������ͭ����������ȫ����ʱ��pH��3.2��ͭ���ӿ�ʼ����ʱ��pH��4.7�����Ե�����Һ��pHӦ����3.2��pH��4.7��
��4���Ȼ�ͭ����ˮCu2��ˮ�⣺Cu2��+2H2O Cu(OH)2+2H�� �����Լ��������Ŀ����������ˮ�⡣
Cu(OH)2+2H�� �����Լ��������Ŀ����������ˮ�⡣
��5��ͭ����ˮ�����ȣ������ɵ��Ȼ��⼫�ӷ�����������CuCl2��Һ���ɵõ��Ĺ�����������ͭ�����յõ���������ͭ������Ҫ�õ��Ȼ�ͭ����Ӧ����HCl������������
���㣺�����Ȼ�ͭ�����Ʊ�ʵ��ԭ�����й��ж��Լ�ˮ��ԭ��Ӧ�õ��й��ж�
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ�����ض�ѧ������֪ʶ�Ĺ�����ѵ��������������ѧ���淶���Ͻ���ʵ���������������ѧ����ѧ������������������Ҫע����Ǹ�����Ҫ��ȷ���������͵�������Ҫ����ʵ���������Ϊ���ģ�ͨ����ʲô��Ϊʲô���������ص㿼��ʵ����������Ĺ淶�Ժ�ȷ�Լ��������֪ʶ���ʵ�������������


 ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||
| ʵ���� | ��ˮ���ʵ���Ũ�� ��mol?L-1�� |
�������ʵ���Ũ�� ��mol?L-1�� |
�����ҺpH |
| �� | 0.1 | 0.1 | pH=5 |
| �� | C | 0.2 | pH=7 |
| �� | 0.2 | 0.1 | pH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||
| c(CuCl 42- ) |
| c[Cu(H2O) 42- ]?c4(Cl-) |
| c(CuCl 42- ) |
| c[Cu(H2O) 42- ]?c4(Cl-) |
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| ||
| ||
| c(CuCl 42- ) |
| c[Cu(H2O) 42+ ]?c4(Cl-) |
| c(CuCl 42- ) |
| c[Cu(H2O) 42+ ]?c4(Cl-) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ��ͨ�к����ظ߶���ѧ����ĩ���Ի�ѧ�Ծ����������� ���ͣ�ʵ����
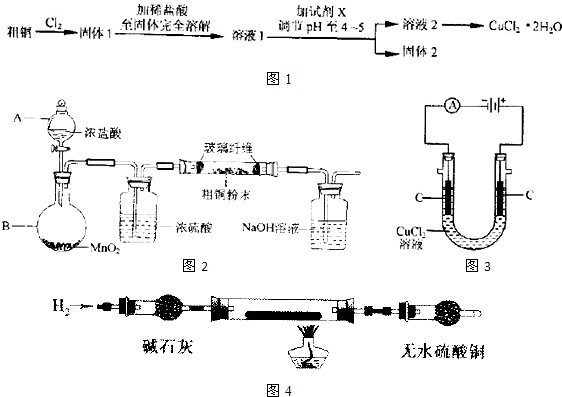
��14�֣��Ȼ�ͭ���壨CuCl2��xH2O������Ҫ�Ļ���ԭ�ϣ��������������������ȡ��ÿ�ȸʯ[��Ҫ��Cu2(OH)2CO3����������Fe��Si�Ļ�����]�Ʊ��Ȼ�ͭ���壬�������£�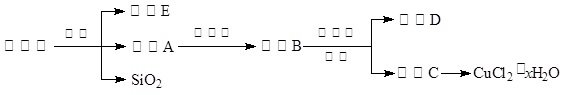
��֪���йؽ������Ӵӿ�ʼ������������ȫʱ��Һ��pH��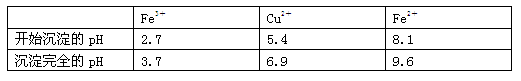
������ʱ��Ϊ����߽�ȡ�ʿɲ�ȡ�Ĵ�ʩ�� ����д��һ�㣩
������ҺA���еĽ���������Cu2����Fe2�������Լ���ΪCl2��ͨ��Cl2������Ӧ�����ӷ���ʽ�� ��
�Ǽ����Լ��ڵ�Ŀ���ǵ���pH��a��a�ķ�Χ�� ��
Ϊ���������������ӣ��Լ��ڿ�ѡ�� ��
| A����ˮ | B������ͭ | C��������ͭ | D���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�콭��ʡ��ͨ�к����ظ߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��14�֣��Ȼ�ͭ���壨CuCl2��xH2O������Ҫ�Ļ���ԭ�ϣ��������������������ȡ��ÿ�ȸʯ[��Ҫ��Cu2(OH)2CO3����������Fe��Si�Ļ�����]�Ʊ��Ȼ�ͭ���壬�������£�
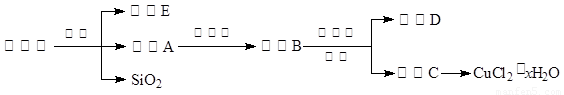
��֪���йؽ������Ӵӿ�ʼ������������ȫʱ��Һ��pH��
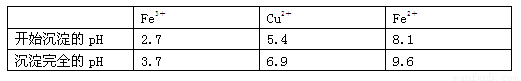
������ʱ��Ϊ����߽�ȡ�ʿɲ�ȡ�Ĵ�ʩ�� ����д��һ�㣩
������ҺA���еĽ���������Cu2����Fe2�������Լ���ΪCl2��ͨ��Cl2������Ӧ�����ӷ���ʽ�� ��
�Ǽ����Լ��ڵ�Ŀ���ǵ���pH��a��a�ķ�Χ�� ��
Ϊ���������������ӣ��Լ��ڿ�ѡ�� ��
A����ˮ B������ͭ C��������ͭ D����������
������ҺC���CuCl2��xH2O��ʵ����������Ǽ���Ũ������ȴ�ᾧ�����˺�ϴ�ӵȲ���������Ũ��������������������Ŀ���ǣ� ��
�ɹ�ҵ�������̻������Cu2���ķ�ˮ�����ˮ��������pH=8���������ˮ��Cu2��Ũ��Ϊ mol/L������֪Ksp[Cu(OH)2]=5.6��10��20��
���Ȼ���ͭ��CuCl��Ҳ��һ����Ҫ�Ļ���ԭ�ϡ�
�Ʊ����̣���CuCl2��Һ��ͨ��һ������SO2������һ��ʱ�������CuCl��ɫ������д���Ʊ�CuCl�����ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com