
有4种碳骨架如下的烃,下列说法正确的是( )
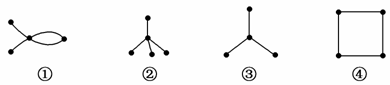
A.①和④互为同素异形体
B.②和③互为同系物
C.①和④都能发生加成反应
D.只有②和③能发生取代反应
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
在溶液中加入足量Na2O2后仍能大量共存的离子组是( )
A.NH4+、Ba2+、Cl-、NO3- B.K+、AlO2-、Cl-、SO42-
C.Ca2+、Mg2+、NO3-、HCO3- D.Na+、Cl-、CO32-、SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下向1L pH=2的醋酸溶液中加入2L pH=2的盐酸,则混合溶液的pH为(假设混合后溶液体积不变,室温下醋酸的电离平衡常数为1.8×10-5)( )
A.2.3 B.1.7 C.2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定体积的密闭容器中,进行如下化学反应CO2(g)+H2(g)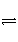
 CO(g)+H2O(g),其
CO(g)+H2O(g),其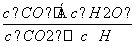 =K,K被称为化学平衡常数,其中K和温度的关系如下表:
=K,K被称为化学平衡常数,其中K和温度的关系如下表:
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
根据以上信息推断以下说法正确的是( )
A.此反应为放热反应
B.此反应只有达到平衡时,密闭容器中的压强才不会变化
C.此反应达到1 000 ℃时的反应速率比700 ℃时大
D.该反应的化学平衡常数越大,反应物的转化率越低
查看答案和解析>>
科目:高中化学 来源: 题型:
A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应起始时,A、B的体积相同。(已知:2NO2(g)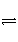
 N2O4(g) ΔH<0)
N2O4(g) ΔH<0)
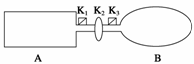
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是vA______vB(填“>”、“<”或“=”);若打开活塞K2,气球B将______(填“变大”、“变小”或“不变”)。
(2)若在A、B中再充入与初始量相等的NO2,则达到平衡时,NO2的转化率αA将________(填“增大”、“减小”或“不变”);若通入等量的Ne气,则达到平衡时,A中NO2的转化率将________,B中NO2的转化率将______(填“变大”、“变小”或“不变”)。
(3)室温下,若A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时,______中的颜色较深。
(4)若在容器A中充入4.6 g的NO2,达到平衡后容器内混合气体的平均相对分子质量为57.5,则平衡时N2O4的物质的量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有机物的命名正确的是( )
A.2,2二甲基3丁烯
B.2,3二甲基3乙基丁烷
C.3,3,5,5四甲基己烷
D.2甲基1,3丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃A 0.2 mol在氧气中充分燃烧后,生成化合物B、C各1.2 mol。
(1)烃A的分子式为________。
(2)若取一定量的A完全燃烧后,生成B、C各3 mol,则有________ g烃A参加了反应,燃烧时消耗标准状况下的O2________L。
(3)若烃A不能使溴水退色,但在一定条件下,能与Cl2发生取代反应,其一氯代物只有一种,则A的结构简式为________。
(4)若烃A能使溴水退色,在催化剂作用下与H2加成,其加成产物分子中含有4个甲基,则A可能的结构简式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下列资料表示了三种金属被人类开发利用的大致年限。
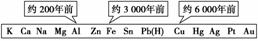
(1)上述资料中的三种常用金属的开发利用之所以有先后,主要取决于________(填选项序号)。
A.金属的导电性强弱
B.金属在地壳中的含量多少
C.金属的化合价高低
D.金属的活动性大小
(2)早在西汉成书的《淮南万毕术》里,就有“曾青得铁则化为铜”的记载。曾青又有空青、白青、石胆、胆矾等名称,其实都是天然的硫酸铜。
①写出“曾青得铁则化为铜”的离子方程式___________________________________________________________________
_________________________________________________________________。
②若根据上述反应设计成原电池,请在方框中画出原电池的装置图,标出正、负极和电解质溶液,并写出电极反应式。

正极反应: ________________________________________________;
负极反应: ______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)===Na2CO3(s)+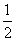 O2(g) ΔH=-226 kJ·mol-1
O2(g) ΔH=-226 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是( )
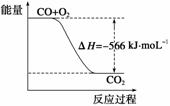
A.CO的燃烧热为283 kJ
B.如图可表示为CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>-452 kJ·mol-1
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com