
【题目】根据能量变化示意图,下列热化学方程式正确的是( )
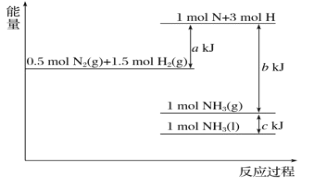
A.N2(g)+3H2(g)=2NH3(g) ΔH=-(b-a)kJ/mol
B.N2(g)+3H2(g)=2NH3(g) ΔH=-(a-b)kJ/mol
C.2NH3(l)=N2(g)+3H2(g) ΔH=2(b+c-a)kJ/mol
D.2NH3(l)=N2(g)+3H2(g) ΔH=2(a+b-c)kJ/mol
【答案】C
【解析】
焓变等于反应物断裂化学键吸收的能量减去形成化学键释放的能量,由图可知,![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) △H=(a-b)kJmol-1,
H2(g)=NH3(g) △H=(a-b)kJmol-1,![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) △H=(a-b-c)kJmol-1,据此分析判断。
H2(g)=NH3(l) △H=(a-b-c)kJmol-1,据此分析判断。
A.![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) △H=(a-b)kJmol-1,则N2(g)+3H2(g)=2NH3(g) △H=-2(b-a)kJmol-1,故A错误;
H2(g)=NH3(g) △H=(a-b)kJmol-1,则N2(g)+3H2(g)=2NH3(g) △H=-2(b-a)kJmol-1,故A错误;
B.![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) △H=(a-b)kJmol-1,则N2(g)+3H2(g)=2NH3(g)△H═-2(b-a)kJmol-1,故B错误;
H2(g)=NH3(g) △H=(a-b)kJmol-1,则N2(g)+3H2(g)=2NH3(g)△H═-2(b-a)kJmol-1,故B错误;
C.![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) △H=(a-b-c)kJmol-1,则N2(g)+3H2(g)=2NH3(l) △H=2(a-b-c)kJmol-1,则2NH3(1)=N2(g)+3H2(g)△H=2(b+c-a)kJmol-1,故C正确;
H2(g)=NH3(l) △H=(a-b-c)kJmol-1,则N2(g)+3H2(g)=2NH3(l) △H=2(a-b-c)kJmol-1,则2NH3(1)=N2(g)+3H2(g)△H=2(b+c-a)kJmol-1,故C正确;
D.![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) △H=(a-b-c)kJmol-1,则N2(g)+3H2(g)=2NH3(l) △H=2(a-b-c)kJmol-1,则2NH3(1)=N2(g)+3H2(g)△H=2(b+c-a)kJmol-1,故D错误;
H2(g)=NH3(l) △H=(a-b-c)kJmol-1,则N2(g)+3H2(g)=2NH3(l) △H=2(a-b-c)kJmol-1,则2NH3(1)=N2(g)+3H2(g)△H=2(b+c-a)kJmol-1,故D错误;
故选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】氮是我们熟悉的典型非金属元素,研究氮及其化合物的性质对于生产、生活、科研具有重要意义,请回答以下问题:
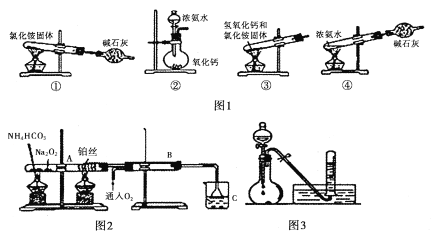
I. (1)图1为制取氨气的装置和选用的试剂,其中合理的是______________(填字母)。
A,①② B. ②③ C. ②④ D. ①③
(2)实验室制备氨气的化学方程式是____________________________________。
II. 图2位铵盐的受热分解装置
(1)被加热的铂丝处发生反应的化学方程式为____________________________________。
(2)B中出现的现象为_______________________________________________________。
(3)如图3:将上述烧杯C中反应得到酸的足量的浓溶液与Cu反应,实验完毕后,试管中收集到气体的主要成分为____________________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图1所示。下列说法正确的是
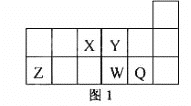
A. 元素X与元素Z的最高正化合价之和的数值等于8
B. 原子半径的大小顺序为:rX>rY>:rZ>rW>rQ
C. 离子Y2-和Z 3+的核外电子数和电子层数都不相同
D. 元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( )

选项 | ① | ② | ③ | 实验结论 |
A | 稀盐酸 | CaCO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
B | 浓硫酸 | 蔗糖 | Ba(NO3)2溶液 | 验证SO2与可溶性钡盐可生成白色沉淀 |
C | 浓氨水 | 生石灰 | 酚酞溶液 | 氨气的水溶液呈碱性 |
D | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是四种原子序数依次增大的短周期元素,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物(ZXY)2的结构式如图所示。下列叙述不正确的是( )
![]()
A.化合物(ZXY)2中Z元素的化合价为-2价
B.Y的氧化物对应的水化物可能是弱酸
C.(ZXY)2分子中X原子的杂化方式为sp杂化
D.X、Y、Z、W四种元素电负性的大小顺序为:Z>Y>X>W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正硼酸(H3BO3)是一种白色晶体,有与石墨相似的层状结构,层内的H3BO3分子通过氢键相连(如图所示)。H3BO3在冷水中溶解度较小,可溶于热水,在水中的解离反应为:H3BO3+H2O![]() H++B(OH)4-。下列有关说法中正确的是( )
H++B(OH)4-。下列有关说法中正确的是( )

A.正硼酸晶体属于原子晶体
B.H3BO3和B(OH)4-中B原子杂化轨道的类型都为sp2
C.H3BO3是三元弱酸
D.含1molH3BO3的晶体中含有3mol氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3、和FeO)得到绿矾(FeSO4·7H2O),在通过绿矾制备铁黄[FeO(OH)]的流程如下:
![]()
已知:FeS2和铁黄均难溶于水
下列说法不正确的是
A. 步骤①,最好用硫酸来溶解烧渣
B. 步骤②,涉及的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+
C. 步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D. 步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是一种重要的化工原料,可发生如下转化。下列说法中不正确的是( )
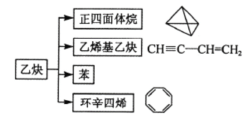
A.以上转化均为加成反应
B.正四面体烷的二氯代物只有1种结构
C.苯乙烯(![]() )和环辛四烯互为同分异构体
)和环辛四烯互为同分异构体
D.等质量的苯和乙烯基乙炔充分燃烧时消耗氧气的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列化学反应的离子方程式的是( )
A.铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑
B.铝粉投入到NaOH溶液中:Al+2OH-=![]() +H2↑
+H2↑
C.氯化铁溶液中加入铁粉:2Fe3++Fe=3Fe2+
D.AlCl3溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com