
| A、1:1 | B、2:1 |
| C、3:1 | D、1:3 |


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
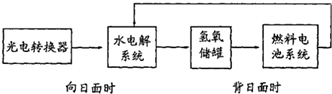 右图是某太空空间站能量转化系统的局部示意图,基中燃料电池采用KOH为电解液,下列有关说法中正确的是( )
右图是某太空空间站能量转化系统的局部示意图,基中燃料电池采用KOH为电解液,下列有关说法中正确的是( )| A、该能量转化系统工作时,需不断补充H2O |
| B、该转化系统的能量本质上来源于太阳能 |
| C、水电解系统中的阴极反应:4OH--4e-=O2+2H2O |
| D、燃料电池放电时的负极反应:H2-2e-=2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素铯的两种核素137Cs比133Cs多四个质子 |
| B、等质量的H2、D2、T2三种气体的电子数之比为2:3:6 |
| C、一种元素只能有一种质量数 |
| D、在氮原子中,质子数为7而中子数不一定为7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学性质相似的有机物一定是同系物 |
| B、分子组成相差一个或几个CH2原子团的有机物一定是同系物 |
| C、若烃中碳、氢元素的质量分数相同,它们必定是同系物 |
| D、互为同分异构体的两种有机物一定不能互称为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com