
【题目】下列各组内物质反应产生的气体分别通入FeSO4溶液中,能与FeSO4发生反应的是( )
A.MnO2与浓盐酸共热B.Al与NaOH溶液
C.食盐和浓硫酸共热D.铜片和浓硫酸共热
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】电子层数相同的三种元素X、Y、Z,已知最高价氧化物对应水化物的酸性HXO4>H2YO4>H3ZO4,则下列判断错误的是 ( )
A. 原子半径X<Y<Z
B. 气态氢化物的稳定性HX>H2Y>ZH3
C. 非金属性Z>Y>X
D. 阴离子的还原性X-<Y2-<Z3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸性KMnO4、H2O2、Fe(NO3)3是重要的氧化剂,用所学知识回答问题:
(1)3H2SO4+2KMnO4+5H2O2===K2SO4+2MnSO4+5O2↑+8H2O,当有6 mol H2SO4参加反应,有________mol还原剂被氧化。
(2)在稀硫酸中,KMnO4与H2C2O4反应的离子方程式为__________________________
(3)Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,再变为棕黄色,溶液先变为浅绿色的离子方程式是_______________ ,再变为棕黄色的原因是_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
A. 一定条件下,将1 mol N2和3 mol H2混合,充分反应后转移的电子数为6 NA
B. 1.5 mol CH4所含的电子数为15 NA
C. 6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2 NA
D. 常温常压下,11.2 L Cl2含氯原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙(CaO2)是一种重要的氧化剂,实验室常用钙单质与氧气在加热条件下反应来制备。下列说法错误的是
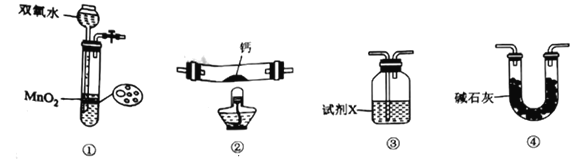
A. 装置①可用于制备氧气
B. 点燃装置②处酒精灯之前,应先排尽装置中的空气
C. 若装置③用于干燥氧气,试剂X可用浓硫酸
D. 装量④可用装置③代替
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ca(OH)2和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小。在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应Ⅰ:WO42—(aq)+ Ca(OH)2(s) ![]() CaWO4(s)+2OH-(aq)。
CaWO4(s)+2OH-(aq)。
(1)如图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线。

①计算T1时Ksp(CaWO4)=________。
②T1________T2(填“>”、“=”或“<”)。
(2)反应Ⅰ的平衡常数K理论值如表所示:
温度/℃ | 25 | 50 | 90 | 100 |
K | 79.96 | 208.06 | 222.88 | 258.05 |
①该反应平衡常数K的表达式为________________。
②该反应的ΔH________0(填“>”、“=”或“<”)。
③由于溶液中离子间的相互作用,实验测得的平衡常数与理论值相距甚远。50℃时,向一定体积的钨酸钠碱性溶液[c(Na2WO4)=c(NaOH)=0.5mol·L-1]中,加入过量Ca(OH)2,反应达到平衡后WO42—的沉淀率为60%,计算实验测得的平衡常数________________。
(3)制取钨酸钙时,适时向反应混合液中添加适量盐酸,分析作用: __________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com