
【题目】除去下列物质中混有的杂质,所选用的试剂及操作方法均正确的是
物质 | 杂质 | 除杂质应选用的试剂和操作方法 | |
A | CO2 | CO | 通入O2,点燃 |
B | NaOH固体 | Na2CO3固体 | 加入过量盐酸,蒸发 |
C | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
D | KNO3溶液 | KOH溶液 | 加入适量的CuSO4溶液,过滤 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,下列叙述正确的是( ) 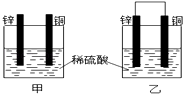
A.装置甲中铜片表面产生气泡
B.装置甲溶液中SO42ˉ向铜片做定向移动
C.装置乙中电子从铜片经导线流向锌片
D.装置乙中正极的电极反应式:2H++2eˉ═H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 乙醇可以被氧化为乙酸,二者都能发生酯化反应
B. 乙醇易燃烧,污染小,只能在实验室中作燃料
C. 常在燃料乙醇中添加少量煤油用于区分食用乙醇和燃料乙醇,因为煤油具有特殊气味
D. 除去乙醇中少量乙酸:加入足量生石灰蒸馏。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素的原子序数依次增大,A的最高价和最低价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道是4s电子数的4倍.请回答下列问题:
(1)F的基态原了价电子排布式为;
(2)B、C、D、E的原子的第一电离能由小到大的顺序为;(用元素符号回答)
(3)下列关于B2A2分子和A2D2分子的说法正确的是;
A.分子中都含有σ键和π键
B.中心原子都sp杂化
C.都是含极性键和非极性键的非极性分子
D.互为等电子体
E.B2A2分子的沸点明显低于A2D2分子
(4)F2+能与BD分子形成[F(BD)4]2+ , 其原因是BD分子中含有;
(5)由B、E、F三种元素形成的一种具有超导性的晶体,晶胞如图所示.B位于E和F原子紧密堆积所形成的空隙当中.与一个F原子距离最近的F原子的数目为 , 该晶体的化学式为 , 若该晶体的相对分子质量为M,阿伏加德罗常数为NA , B、E、F三种元素的原子半径分别为r1pm、r2pm、r3pm,则该晶体的密度表达式为 . 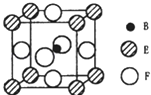
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属材料是人类社会发展的重要物质基础。下列说法正确的是
A.钛及钛合金是目前使用量最大的金属材料
B.镁是一种国防金属,电解熔融MgCl2可得到单质镁
C.铝合金大量用于高铁建设,铝可用CO还原Al2O得到
D.稀土(钇、钪及镧系)是战略金属,稀土元素均位于ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐泥是氯碱工业中的废渣,主要成分是镁的硅酸盐和碳酸盐(含少量铁、铝、钙的盐).实验室以盐泥为原料制取MgSO47H2O的实验过程如下: 29.0g盐泥 ![]()
![]() 滤液Ⅰ→滤液Ⅱ→产品
滤液Ⅰ→滤液Ⅱ→产品
已知:①室温下Ksp[Mg(OH)2]=6.0×10﹣12 . ②在溶液中,Fe2+、Fe3+、Al3+从开始沉淀到沉淀完全的pH范围依次为7.1~9.6、2.0~3.7、3.1~4.7.③三种化合物的溶解度(S)随温度变化的曲线如图所示.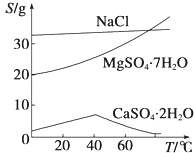
(1)在盐泥中加入稀硫酸调pH为1~2以及煮沸的目的是;
(2)若室温下的溶液中Mg2+的浓度为6.0molL﹣1 , 则溶液pH≥才可能产生Mg(OH)2沉淀.
(3)由滤液Ⅰ到滤液Ⅱ需先加入NaClO调溶液pH约为5,再趁热过滤,则趁热过滤的目的是 , 滤渣的主要成分是;
(4)从滤液Ⅱ中获得MgSO47H2O晶体的实验步骤依次为①向滤液Ⅱ中加入; ②过滤,得沉淀;③;④蒸发浓缩,降温结晶;⑤过滤、洗涤得产品.
(5)若获得的MgSO47H2O的质量为24.6g,则该盐泥中镁[以Mg(OH)2计]的百分含量约为(MgSO47H2O的相对分子质量为246).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空:
(1)AlCl3溶液蒸干并灼烧得到的物质是(填化学式).
(2)泡沫灭火器灭火时发生反应的离子方程是;
(3)已知25℃时,Ksp[Cu(OH)2]=2×10﹣20 , 某CuSO4溶液里c(Cu2+)=0.02molL﹣1 , 如要生成Cu(OH)2 沉淀,应调整溶液的pH,使之大于 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。
①把FeO、Fe2O3先溶于足量的稀盐酸中、再通入适量的氯气则可制取FeCl3溶液。FeO、Fe2O3溶于足量的稀盐酸中,在上述溶液中通入适量的氯气时发生的反应的离子方程式为。若要检验溶液中Fe3+存在应选用的试剂是。
②写出FeCl3溶液与金属铜发生反应的化学方程式 , 当转移电子数为6.02×1024时,被氧化的物质的质量为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,(如图1),加热回流一段时间后换成蒸馏装置(如图2)进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品,请回答下列问题: 
(1)在图1烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入 , 目的是 .
(2)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图是分离操作步骤流程图,请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法.试剂a是 , 试剂b是;
分离方法①是 , 分离方法②是 , 分离方法③是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com