
| A. | SO2 | B. | NH3 | C. | N2 | D. | CO2 |
分析 用干燥剂干燥气体时,总的原则是:中性干燥剂既可以用来干燥酸性气体又可以用来干燥碱性气体;酸性干燥剂不能用来干燥碱性气体;碱性干燥剂不能用来干燥酸性气体,注意浓硫酸具有强氧化性,能够由于干燥具有较强还原性的气体,如硫化氢.
解答 解:A.二氧化硫为酸性氧化物,能够与碱石灰反应,不能使用碱石灰干燥,故A错误;
B.氨气为碱性气体,不能用浓硫酸干燥,故B错误;
C.氮气为中性气体,既能用浓硫酸干燥又能用碱石灰干燥,故C正确;
D.二氧化碳是酸性物质,能和碱石灰反应,所以不能用碱石灰干燥,故D错误;
故选C.
点评 本题考查常见气体的性质及干燥剂的选用,题目难度不大,明确常见气体的性质及干燥剂的特点为解答关键,试题培养了学生灵活应用基础知识的能力.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 200 mL 2 mol•L-1HCl | B. | 100 mL 2 mol•L-1H2SO4 | ||
| C. | 100 mL 3 mol•L-1 HCl | D. | 50 mL 18.4 mol•L-1H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
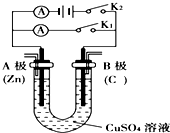 请按要求回答下列问题.
请按要求回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
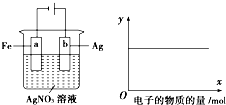 按图实验,若x轴表示流入阴极电子的物质的量,则y轴可表示①c(Ag+) ②c(NO3-)③a棒的质量④b棒的质量( )
按图实验,若x轴表示流入阴极电子的物质的量,则y轴可表示①c(Ag+) ②c(NO3-)③a棒的质量④b棒的质量( )| A. | ①③ | B. | ③④ | C. | ①②④ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
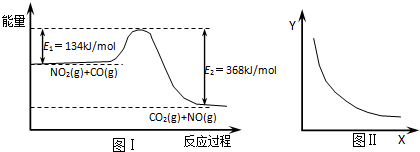
| A. | 该反应的焓变△H=234kJ/mol | |
| B. | 若X表示CO的起始浓度,则Y表示的可能是NO2的转化率 | |
| C. | 若X表示反应时间,则Y表示的可能是混合气体的密度 | |
| D. | 若X表示温度,则Y表示的可能是CO2的物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取少量试液,加入用盐酸酸化的氯化钡溶液,有白色沉淀生成 | |
| B. | 取少量试液,加入氯化钡溶液,有白色沉淀生成,再加稀硝酸沉淀不消失 | |
| C. | 取少量试液,加入硝酸钡溶液,有白色沉淀生成 | |
| D. | 取少量试液,加入盐酸无现象,再加氯化钡溶液,有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com