

请填写下列空白:
(1)写出实验中Na2O2和Na2O分别发生反应的化学方程式____________________________。
(2)完成该实验所需的装置是(填标号)_______________。
(3)所选用的装置的连接顺序是_______________(填各接口的字母,连接用的胶管可以省略)。
解析:解答此题首先要迅速联想起氧化钠和过氧化钠的化学性质:
(1)Na2O+H2O![]() 2NaOH
2NaOH
2Na2O2+2H2O![]() 4NaOH+O2↑
4NaOH+O2↑
(2)Na2O+CO2![]() Na2CO3
Na2CO3
2Na2O2+2CO2![]() 2Na2CO3+O2
2Na2CO3+O2
此实验设计的原理即利用Na2O、Na2O2性质的差异:Na2O2与水或CO2反应生成O2,而Na2O不生成O2。若能测得O2的量,按照反应式就可以计算出Na2O2的质量。对所给反应物进行分析,CaCO3和盐酸是用于制CO2的,这样此题就可能有两种方法:一种是用Na2O2和H2O反应制O2;另一种是用Na2O2和CO2反应,然后用排水法收集气体,测定其体积。因此选用这两个反应中的任一个,都可测定Na2O2的纯度。根据题目要求应采用与水反应,因为根据这一反应原理设计的实验装置较另一方案简单。需要的实验装置是⑤①④,装置的连接顺序是G接A,B接F。
答案:(1)Na2O+H2O![]() 2NaOH
2NaOH
2Na2O2+2H2O![]() 4NaOH+O2↑
4NaOH+O2↑
(2)⑤①④
(3)G接A,B接F


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:物理教研室 题型:022
①NaOH溶液吸收法,反应原理如下:
2NO2+2NaOH====NaNO2+NaNO3+H2O
NO2+NO+2NaOH====2NaNO2+H2O
②氨催化还原法,反应原理是:
![]()
![]()
![]()
现有一定量的含NO2和NO的HNO3工业尾气(不含其他气体),若用过量的NaOH溶液吸收后,溶液中NaNO3与NaNO2的物质的量之比恰好与尾气中NO和NO2的物质的量之比相等。
(1)若用NOx表示该尾气中氮的氧化物的平均组成,试求x的值。
(2)若1体积的该尾气用氨催化还原法处理,至少消耗多少体积相同状况下的氨气?
查看答案和解析>>
科目:高中化学 来源:必修一导学指导化学鲁科版 鲁科版 题型:058
现有一定量的含Na2O杂质的Na2O2试样,请从下图中选用适当的实验装置,设计一个最简单的实验,测定Na2O2试样的纯度(可供选用的反应物只有CaCO3固体、20%盐酸和蒸馏水).(已知此状况下O2、CO2的密度分别为1.429 g·L-1,1.977 g·L-1)
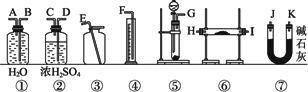
请填写下列空白:
(1)写出实验中Na2O2和Na2O分别发生反应的化学方程式________.
(2)完成该实验所需的装置是(填标号)________.
(3)所选用的装置的连接顺序是________(填各接口的字母,连接用的胶管可以省略).
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸工业中尾气的N的氧化物(NO,NO2)是主要的大气污染之一,其常用的治理方法中有以下两种(已简化)。
NaOH吸收法,反应原理如下:
2NO2+2NaOH=NaNO3+NaNO2+H2O
氨催化还原法,反应原理是:
![]()
现有一定量的含NO2和NO的硝酸工业尾气(不含其他气体),若用过量的NaOH吸收后,溶液中NaNO3和NaNO2的物质的量之比恰好与原尾气中NO和NO2的物质的量之比相等。
(1)若用NOx表示该尾气中氮的氧化物的平均组成,试求x的值。
x=__________________________________________。
(2)将1体积的该尾气用②的方法处理,至少消耗相同状况下的NH3的体积为____________。
(3)配平下列方程式:
______NOx+_____NH3=______N2+_____H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸工业尾气中的氮的氧化物(NO、NO2)是主要的大气污染物,其常用的治理方法有以下两种(已简化)
①NaOH吸收法反应原理如下:2 NO2+2NaOH=NaNO3+NaNO2+H2O;NO+NO2+2NaOH=2NaNO2+ H2O
②氨催化还原法 反应原理是:NO2+NH3→N2+H2O
现有一定量的含NO2和NO的硝酸工业尾气(不含其他气体);若用过量的NaOH溶液吸收后溶液中 NaNO3与 NaNO2的物质的量之比恰好与尾气中NO和 NO2的物质的量之比相等。
(1)若用NOx表示该尾气中氮的氧化物的平均组成,试求x的值。
(2)将1体积的该尾气用氨催化还原法处理,至少消耗相同状况下多少体积的氨气?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com