
下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据。
| 元素 | I1/eV | I2/eV | I3/eV[ |
| 甲 | 5.7 | 47.4 | 71.8 |
| 乙 | 7.7 | 15.1 | 80.3 |
| 丙 | 13.0 | 23.9 | 40.0 |
| 丁 | 15.7 | 27.6 | 40.7 |
科目:高中化学 来源: 题型:单选题
六种短周期元素(a、b、c、d、e、f)的原子序数依次增大。其中a与e同主族,b与f同主族,e与f同周期;常温下a、e的单质状态不同;d的核电荷数是b的最外层电子数的2倍;单质f是一种重要的半导体材料。由此可推知
| A.a、c两种元素只能组成化学式为ca3的化合物 |
| B.b、c、d分别与a形成的化合物,沸点由高到低依次为:d>c>b |
| C.原子半径由大到小的顺序是 e>f>b>c>a |
| D.元素的非金属性由强到弱的顺序是 d>c>f>b |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是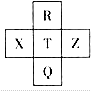
| A.非金属性:Z>T>X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R<T<Q |
| D.R、T、Q的最高正价相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
若某一个原子在处于能量最低状态时,外围电子排布为4d15s2,则下列各项说法正确的是
| A.该元素原子最外层共有3个电子 |
| B.该元素位于第5周期ⅡA族 |
| C.该元素原子核外第N层上共有9个不同状态的电子 |
| D.该元素原子第四电子层上有5个空轨道 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于氢原子电子云图的说法正确的是
| A.通常用小黑点来表示电子的多少,黑点密度大,电子数目大 |
| B.黑点密度大,单位体积内电子出现的机会大 |
| C.通常用小黑点来表示电子绕核作高速圆周运动 |
| D.电子云图是对电子运动无规律性的描述 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有A、B、C、D、E五种短周期元素,A是地壳中含量最多的元素,B元素有3种同位素B1、B2、B3,B3原子的质量数是B1的3倍,C是非金属性最强的元素,D和C可以形成DC型离子化合物,且离子的电子层结构相同,E元素原子的最外层电子数比内层电子总数少6个。下列说法正确的是
A.离子半径:D+>C-
B.EA2是光导纤维的主要成分
C.A和B可以形成原子个数比1∶1的化合物
D.以上元素中形成的最高价氧化物对应的水化物酸性最强的是C
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质。已知:甲+乙=丁+辛,甲+丙=戊+辛;常温下0.1 mol/L 丁溶液的pH为13。下列说法正确的是( )
A.元素B在周期表中的位置为第二周期第VIA族
B.元素B、C、D的原子半径由大到小的顺序为r (D)>r(C)>r(B)
C.1.0 L、0. 1 mol/L戊溶液中阴离子总的物质的量小于0. 1 mol
D.1 mol甲与足量的乙完全反应共转移了约6.02×1023个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com