
��14�֣�ÿ��2�֣�
I���ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�����塣��ԭ��Ϊ��
N2(g)+3H2(g) 2NH3(g) ��H= -92.4 kJ/mol �ݴ˻ش��������⣺
��1��Ϊ����߰����IJ��ʣ�����ѡ��ķ����� _______ ������ţ���ѡ�۷֣���
�� �����¶� �� ����ѹǿ �� ʹ�ô��� �� ��ʱ�����NH3
��2�������ܱ������н��еĿ��淴Ӧ��N2(g)+3H2(g)2NH3(g)��������������£�
˵���÷�Ӧ�Ѿ��ﵽ��ѧƽ��״̬____________________________________��
��N2������Ӧ������NH3���淴Ӧ���ʵ�1/2
���ں��������£���������ѹǿ���ֲ���
��N2��H2��NH3�����ʵ���֮��Ϊ1��3��2
�ܵ�λʱ����ÿ����3mol H2��ͬʱ��2mol NH3����
��3mol N-N�����ѣ�ͬʱ��6mol N-H������
��3��һ�������£�NH3�ڹ̶�������ܱ������з����ֽⷴӦ����H��0������ƽ����ı��±��з�Ӧ����x����ƽ����ϵ����x����y�ݼ����ǣߣߣߣ�____________��ѡ����ţ���
| ѡ�� | a | b | c | d |
| x | �¶� | �¶� | ����H2�����ʵ��� | ����NH3�����ʵ��� |
| y | NH3�����ʵ��� | ƽ�ⳣ��K | NH3��ת���� | ���������ʵ����ܺ� |
II����1����������Һ�У������(KIO3)���������ƿɷ������·�Ӧ��
2IO3����5SO32����2H��===I2��5SO42����H2O
���ɵĵ�����õ�����Һ���飬���ݷ�Ӧ��Һ������ɫ�����ʱ���������÷�Ӧ�����ʡ�
ijͬѧ���ʵ�����±���ʾ��
|
| 0.01mol��L��1 KIO3������Һ(������)�����/mL | 0.01mol��L��1 Na2SO3��Һ�����/mL | H2O����� /mL | ʵ�� �¶� /�� | ��Һ������ɫʱ����ʱ��/s |
| ʵ��1 | 5 | V1 | 35 | 25 | --------- |
| ʵ��2 | 5 | 5 | 40 | 25 | ---------- |
| ʵ��3 | 5 | 5 | V2 | 0 | ----------- |
��ʵ���Ŀ����_______________________________________________________________
________________________________________________��
����V1=___________mL.
��2�����淴ӦC(s)+H2O(g) H2(g)+CO(g)����H>0�ﵽƽ��ı�ijһ������������ı����ʵ����������£�����Ӧ����
![]() ��ʱ��t�Ĺ�ϵ����ͼ��
��ʱ��t�Ĺ�ϵ����ͼ��
��ͼ��t4��t6��ʱ����ƽ���ƶ������������� ��
��ͼ�б�ʾƽ��������CO�ĺ�����ߵ�һ��ʱ���� ��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��14�֣�ÿ��2�֣���֪X��Y��Z���Ƕ����ڵ�Ԫ�أ����ǵ�ԭ���������ε�����X ԭ�ӵĵ��Ӳ��������ĺ������������ͬ����Z ԭ�ӵ������������Ǵ�����������Y �� Z �����γ��������ϵ���̬�������
��1��X ������������������������Y��������������������������Z������������������������������Ԫ��������д��
��2����Y �� Z ��ɣ���Y�� Z��������Ϊ7��12�Ļ�����Ļ�ѧʽ������ʽ���� _____
��3����X��Y��Z�е�����Ԫ����ɣ�����X2Z ���Ӿ�����ͬ������������������ _____ ������������������ _____ �������������������������ӷ��ţ�
��4��X��Y��Z�����γ�һ���Σ�������X��Y��ZԪ�ص�ԭ�ӵĸ�����Ϊ4 ��2 ��3 �����εĻ�ѧʽ�� _____ ����������������������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�����ʡ����Ͽ�и�����ѧ�ڵ��п��Ի�ѧ�Ծ� ���ͣ������
��14�֣�ÿ��2�֣��о�NO2��SO2 ��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1��NO2����ˮ���գ���Ӧ�Ļ�ѧ��Ӧ����ʽΪ �����÷�Ӧ
6NO2�� 8NH3 7N2��12
7N2��12 H2OҲ�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������ L��
H2OҲ�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������ L��
��2����֪��2SO2��g��+O2 ��g��
��g�� 2SO3��g�� ��H="-196.6" kJ��mol-1
2SO3��g�� ��H="-196.6" kJ��mol-1
2NO��g��+O2��g�� 2NO2��g�� ��H="-113.0" kJ��mol-1
2NO2��g�� ��H="-113.0" kJ��mol-1
��д��NO2����SO2���Ȼ�ѧ����ʽ
��һ�������£���NO2��SO2�������1:2�����ܱ������з���������Ӧ��������˵�� ��Ӧ�ﵽƽ��״̬���� ��
��Ӧ�ﵽƽ��״̬���� ��
a����ϵѹǿ���ֲ��� b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ��� d��ÿ����1 mol SO3��ͬʱ����1 molNO2
�۲��������Ӧƽ��ʱNO2��SO2�����Ϊ1:6����ƽ�ⳣ��K�� ��
��3��CO�����ںϳɼ״�����Ӧ����ʽΪCO��g��+2H2��g�� CH3OH��g����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ����ͼ��ʾ��
CH3OH��g����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ����ͼ��ʾ��
�÷�Ӧ��H 0���>���� <������ʵ����������������250�桢1.3��104kPa���ң�ѡ���ѹǿ�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012��ѧ����ʡ����һ�и߶���ѧ�����п��Ի�ѧ�Ծ� ���ͣ������
��14�֣�ÿ��2�֣�
I����1L������ͨ��CO2��H2��2mol����һ�������·�����Ӧ��CO2 + H2 CO + H2O��
CO + H2O��
�ش��������⣺
��1����830�������£���Ӧ�ﵽƽ��ʱCO2��ת����Ϊ50%�����������ƽ�ⳣ��K1=________��
��2���ڣ�1���Ļ����ϣ�����ϵ�¶Ƚ���800�档��֪�������µ�ƽ�ⳣ��K2=0.81��������֪ �÷�Ӧ������ӦΪ___________��Ӧ������ȡ��������ȡ�����
��3���ڣ�1���Ļ����ϣ�ѹ���������֮0.5 L���������µ�ƽ�ⳣ��ΪK3����K3________K1
L���������µ�ƽ�ⳣ��ΪK3����K3________K1
��4��T��ʱ��ijʱ�̲����ϵ�и����ʵ������£�n��CO2 ��=1.2mol��n��H2��=1.5mol��
��=1.2mol��n��H2��=1.5mol��
n��CO��=0.9mol��n��H2O��=0.9mol�����ʱ�÷�Ӧ ����.
���������Ӧ�������淴Ӧ������ƽ��״̬������
II����һ�ݻ�Ϊ1L ���� �������м���һ������X��Y��������ѧ��ӦX(g)��2Y(s)
�������м���һ������X��Y��������ѧ��ӦX(g)��2Y(s)  2Z(g)����H��0����ͼ��������X��Z�����ʵ���Ũ����ʱ��仯�����ߡ�
2Z(g)����H��0����ͼ��������X��Z�����ʵ���Ũ����ʱ��仯�����ߡ�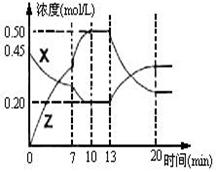
(1)0��10min �����������ѹǿ�� ___________��
����������С������ȷ������
(2)�Ʋ��ڵ�7minʱ���߱仯��ԭ������� ___
��13minʱ���߱仯��ԭ�������  __������ţ�
__������ţ�
������Z���� ������X���� ������
�ܽ��� ��ʹ�ô���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�갲��ʡ������һѧ�����п��Ի�ѧ�Ծ� ���ͣ�ʵ����
��14�֣�ÿ��2�֣�ij�Լ���������������ͭ�������ᣨ��Fe3+����Ӧ��ȡ���������������£�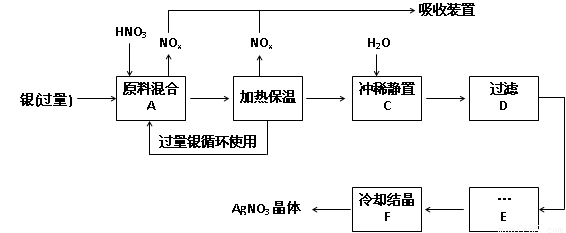
��1����ҵ��һ��ѡ���е�Ũ�ȵ����������Ӧ����ȡ�������������±��ո���ա�
|
|
�ŵ� |
ȱ�� |
|
ʹ��Ũ���� |
��Ӧ���ʿ� |
��Ľϴ���NOx�����϶� |
|
ʹ��ϡ���� |
|
|
��2������B���ȱ��µ������� ��
a�� �����ڼӿ췴Ӧ����
b��������δ��Ӧ������ӷ�
c�������������ַ�Ӧ��������Һ��H+��Ũ��
��3������C��Ϊ�˳�ȥFe3+��Cu2+�����ʣ���ϡʱ����������ԭ���� ��
��4������C�м�ˮ����Ӧ������������������ˮ���Ժ���������ɵIJ���Ӱ���ǣ�
��
��5������E���еIJ����� ��
��6���Ƶõ��������к�����������ͭ��ͨ����ȥ����ͭ�ķ������ڲ���E֮ǰ���������Ƶ�Ag2O��ʹCu2+ת��ΪCu(OH)2��������Ӧ����˳�ȥ���÷�Ӧ�Ļ�ѧ����ʽΪ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012��ѧ����ʡ�߶���ѧ�����п��Ի�ѧ�Ծ� ���ͣ������
��14�֣�ÿ��2�֣�
I����1L������ͨ��CO2��H2��2mol����һ�������·�����Ӧ��CO2 + H2 CO + H2O��
CO + H2O��
�ش��������⣺
��1����830�������£���Ӧ�ﵽƽ��ʱCO2��ת����Ϊ50%�����������ƽ�ⳣ��K1=________��
��2���ڣ�1���Ļ����ϣ�����ϵ�¶Ƚ���800�档��֪�������µ�ƽ�ⳣ��K2=0.81��������֪ �÷�Ӧ������ӦΪ___________��Ӧ������ȡ��������ȡ�����
��3���ڣ�1���Ļ����ϣ�ѹ���������֮0.5L���������µ�ƽ�ⳣ��ΪK3����K3________K1
��4��T��ʱ��ijʱ�̲����ϵ�и����ʵ������£�n��CO2��=1.2mol��n��H2��=1.5mol��
n��CO��=0.9mol��n��H2O��=0.9mol�����ʱ�÷�Ӧ ����.
���������Ӧ�������淴Ӧ������ƽ��״̬������
II����һ�ݻ�Ϊ1L ���ܱ������м���һ������X��Y��������ѧ��ӦX(g)��2Y(s)  2Z(g)����H��0����ͼ��������X��Z�����ʵ���Ũ����ʱ��仯�����ߡ�
2Z(g)����H��0����ͼ��������X��Z�����ʵ���Ũ����ʱ��仯�����ߡ�
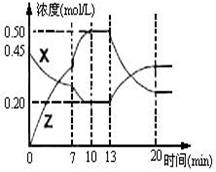
(1)0��10min �����������ѹǿ�� ___________��
����������С������ȷ������
(2)�Ʋ��ڵ�7minʱ���߱仯��ԭ������� ___
��13minʱ���߱仯��ԭ������� __������ţ�
������Z���� ������X���� ������
�ܽ��� ��ʹ�ô���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com