
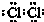 .
.分析 (1)氯气是氯原子间形成一对共用电子对形成的分子;
(2)电解饱和食盐水生成氢氧化钠、氢气和氯气;
(3)使溶液中的平衡正向移动的方法有:升温(吸热反应)或降温(放热反应)、增大反应物浓度、降低生成物浓度(加可与生成物反应的物质);
(4)①根据题目信息“生成可以杀菌消毒的物质”可知一种产物为HClO,根据守恒的原则,另一种产物为NH3;
②只有Cl元素化合价发生变化,氯气的物质的量为0.5mol,化合价分别由0价变化为-1价、+1价.
解答 解:(1)氯气是氯原子间形成一对共用电子对形成的分子,氯气的电子式为: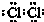 ,
,
故答案为: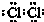 ;
;
(2)电解饱和食盐水制氯气,反应生成氢氧化钠、氢气和氯气,反应的离子方程式为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑;
故答案为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑;
(3)使溶液中的平衡正向移动的方法有:升温(吸热反应)或降温(放热反应)、增大反应物浓度、降低生成物浓度(加可与生成物反应的物质),可加入碳酸钙后氢氧化钠,可使平衡正向移动,
故答案为:ab;
(4)①根据题目信息“生成可以杀菌消毒的物质”可知一种产物为HClO,根据守恒的原则,另一种产物为NH3,方程式为NH2Cl+H2O=HClO+NH3,
故答案为:NH2Cl+H2O=HClO+NH3;
②只有Cl元素化合价发生变化,氯气的物质的量为0.5mol,化合价分别由0价变化为-1价、+1价,则转移电子0.5mol,故答案为:0.5;
点评 本题综合考查元素化合物与基本理论知识,为高考常见题型,侧重于学生的分析、计算能力的考查,注意把握电极方程式的书写以及盐类水解的原理,难度不大.


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学兴趣小组,拟探究和比较SO2和 Cl2的漂白性,设计如图所示的实验装置二套.请你参与探究并回答下列问题.
某化学兴趣小组,拟探究和比较SO2和 Cl2的漂白性,设计如图所示的实验装置二套.请你参与探究并回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应开始到10s,用Z表示的反应速率为0.158 mol•L-1•s-1 | |
| B. | 反应开始到10s,X的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应开始到10s,Y的物质的量的减少是0.79mol | |
| D. | 反应的化学方程式为:X(g)+Y(g)?Z(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com