
.(14分) 硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素完全氧化,剩余的I2用Na2S2O3标准溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
C6H8O6+I2===C6H6O6+2H++2I- 2S2O32-+I2===S4O62-+2I-
在一定体积的某维生素C溶液中加入1.2molL-1 I2溶液25ml,充分反应后,用1.0molL-1Na2S2O3标准溶液滴定剩余的I2。请回答下列问题:
(1)配制100mL 1.0molL-1 Na2S2O3标准溶液,使用的仪器除天平、药匙、胶头滴管外,还需要___________________________________;配制时,用胶头滴管加水定容至刻度线并盖上瓶塞后的下一步操作是_______________________________________
(2)滴定时,可选择_________________作指示剂。滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_____________________________________。直到出现________________________________________现象为止。
(3)若滴定开始和结束时,滴定管中的液面如图所示。反应消耗Na2S2O3标准溶液的体积是_______________。试根据该实验数据计算该溶液中维生素C的物质的量: mol。

(4)判断下列操作对该溶液中维生素C的物质的量测定结果的影响(填“偏高”、“偏低”或“无影响”)
若在配制标准溶液过程中,烧杯中的Na2S2O3溶液有少量溅出,使测定结果_______;
若在滴定终点读取滴定管刻度时,仰视标准液液面,使测定结果_________
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:
.(14分) 硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素完全氧化,剩余的I2用Na2S2O3标准溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
C6H8O6+I2===C6H6O6+2H++2I- 2S2O32-+I2===S4O62-+2I-
在一定体积的某维生素C溶液中加入1.2molL-1 I2溶液25ml,充分反应后,用1.0molL-1Na2S2O3标准溶液滴定剩余的I2。请回答下列问题:
(1)配制100mL 1.0molL-1 Na2S2O3标准溶液,使用的仪器除天平、药匙、胶头滴管外,还需要___________________________________;配制时,用胶头滴管加水定容至刻度线并盖上瓶塞后的下一步操作是_______________________________________
(2)滴定时,可选择_________________作指示剂。滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_____________________________________。直到出现________________________________________现象为止。
(3)若滴定开始和结束时,滴定管中的液面如图所示。反应消耗Na2S2O3标准溶液的体积是_______________。试根据该实验数据计算该溶液中维生素C的物质的量: mol。
(4)判断下列操作对该溶液中维生素C的物质的量测定结果的影响(填“偏高”、“偏低”或“无影响”)
若在配制标准溶液过程中,烧杯中的Na2S2O3溶液有少量溅出,使测定结果_______;
若在滴定终点读取滴定管刻度时,仰视标准液液面,使测定结果_________
查看答案和解析>>
科目:高中化学 来源:2012届福建省厦门六中高三12月月考化学试卷 题型:实验题
.(14分) 硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素完全氧化,剩余的I2用Na2S2O3标准溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
C6H8O6+I2===C6H6O6+2H++2I- 2S2O32-+I2===S4O62-+2I-
在一定体积的某维生素C溶液中加入1.2molL-1 I2溶液25ml,充分反应后,用1.0molL-1Na2S2O3标准溶液滴定剩余的I2。请回答下列问题:
(1)配制100mL 1.0molL-1 Na2S2O3标准溶液,使用的仪器除天平、药匙、胶头滴管外,还需要___________________________________;配制时,用胶头滴管加水定容至刻度线并盖上瓶塞后的下一步操作是_______________________________________
(2)滴定时,可选择_________________作指示剂。滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_____________________________________。直到出现________________________________________现象为止。
(3)若滴定开始和结束时,滴定管中的液面如图所示。反应消耗Na2S2O3标准溶液的体积是_______________。试根据该实验数据计算该溶液中维生素C的物质的量: mol。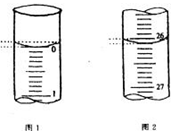
(4)判断下列操作对该溶液中维生素C的物质的量测定结果的影响(填“偏高”、“偏低”或“无影响”)
若在配制标准溶液过程中,烧杯中的Na2S2O3溶液有少量溅出,使测定结果_______;
若在滴定终点读取滴定管刻度时,仰视标准液液面,使测定结果_________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com