
(8分)Ⅰ.已知某反应A(g)+B(g)  C (g)+D(g),过程中的能量变化如图所示,回答下列问题。
C (g)+D(g),过程中的能量变化如图所示,回答下列问题。
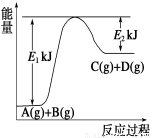
(1)该反应是______________反应(填“吸热”或“放热”),该反应的ΔH=____________kJ·mol-1(用含E1、E2的代数式表示),1 mol气体A和1 mol气体B具有的总能量比1 mol气体C和1 mol气体D具有的总能量____________(填“一定高”、“一定低”或“高低不一定”)。
(2)若在反应体系中加入催化剂使逆反应速率增大,则E1和E2的变化是:E1______,E2_________,ΔH_________(填“增大”“减小”或“不变”)。
Ⅱ.已知下列热化学方程式
Fe2O3(s)+3CO(g) ===2Fe(s)+3CO2(g) ΔH1=-25 kJ·mol-1 ①
3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g) ΔH2=-47 kJ·mol-1 ②
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH3=+19 kJ·mol-1 ③
写出FeO(s)被CO还原成Fe和CO2的热化学方程式_______________________________________。
I(1)吸热;(E1-E2);一定低
(2)减小;减小;不变
II FeO(s)+CO(g)=Fe(s)+CO2(g) ΔH=-11kJ/mol
【解析】
试题分析:I(1)该反应的反应物的总能量低于生成物的总能量,所以是吸热反应,则该反应的ΔH=+(E1-E2)kJ/mol;因为该反应是吸热反应,所以1 mol气体A和1 mol气体B具有的总能量比1 mol气体C和1 mol气体D具有的总能量一定低;
(2)若在反应体系中加入催化剂使逆反应速率增大,催化剂只能降低反应的活化能,而反应热不变,则E1减小,E2减小,ΔH不变;
II根据盖斯定律可知,将已知热化学方程式中的氧化铁、四氧化三铁消去,可得所求方程式,所以FeO(s)+CO(g)=Fe(s)+CO2(g)的热效应ΔH=[①×3-(②+③×2)]/6=[3ΔH1-(ΔH2+2ΔH3)]/6=-11kJ/mol,则eO(s)被CO还原成Fe和CO2的热化学方程式为FeO(s)+CO(g)=Fe(s)+CO2(g) ΔH=-11kJ/mol。
考点:考查化学反应与能量的关系,热化学方程式的书写


科目:高中化学 来源:2014-2015学年山东省乐陵市高二上学期期中考试化学试卷(解析版) 题型:填空题
(8分)研究CO2的利用对促进低碳社会的构建具有重要的意义。
(I)将CO2与焦炭作用生成CO,CO可用于炼铁等。
①已知:Fe2O3(s) + 3C(石墨) =2Fe(s) + 3CO(g) △H 1 =+489 kJ·mol-1
C(石墨) +CO2 (g) =2CO(g) △H 2 = +172 kJ·mol-1
则Fe2O3(s) + 3CO(g) = 2Fe (s) + 3CO2(g) △H= 。
②利用燃烧反应可设计成CO/O2燃料电池(以H2SO4溶液为 电解质溶液),写出该电池的正极反式 。
(II)如图所示,烧杯中都盛有稀硫酸。
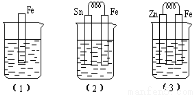
(1)中反应的离子方程式为 ;比较(1)、(2)、(3)中纯铁被腐蚀的速率由快到慢的顺序是 (用序号表示) 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东桓台第二中学高二上学期(10月)检测化学试卷(解析版) 题型:选择题
在下列反应中,水既不是氧化剂又不是还原剂的是 ( )
A.F2 + H2O (生成F2和HF) B.Na + H2O
C.NaH + H2O(生成H2和NaOH) D.Na2O2 + H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东桓台第二中学高一上学期(10月)检测化学试卷(解析版) 题型:选择题
下列说法中正确的是( )
A.纯净物一定由分子构成 B.同种分子构成的物质一定是纯净物
C.混合物肯定由两种以上元素组成 D.含有氧元素的化合物都是氧化物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东桓台第二中学高一上学期(10月)检测化学试卷(解析版) 题型:选择题
用pH试纸测定某一溶液的pH时,规范的操作是( )
A.将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较
B.将溶液倒在pH试纸上,跟标准比色卡比较
C.用干燥洁净的玻璃棒蘸取溶液,滴在pH试纸上,跟标准比色卡比较
D.在试管内放少量溶液,煮沸,把pH试纸放在管口,观察颜色,跟标准比色卡比较
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东安丘市期中考试高二化学模拟(B)卷(解析版) 题型:选择题
对已经达到化学平衡的下列反应: 2X(g)+Y(g)  2Z(g),减小压强时 ( )
2Z(g),减小压强时 ( )
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东安丘市期中考试高二化学模拟(B)卷(解析版) 题型:选择题
由下图分析,有关叙述正确的是( )

A.A―→B+C和B+C―→A两个反应吸收或放出的能量不等
B.A―→B+C是放热反应
C.A具有的能量高于B和C具有的能量总和
D.A―→B+C是吸热反应,则B+C―→A必然是放热反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东安丘市期中考试高二化学模拟(A)卷(解析版) 题型:选择题
如图所示,是在其他条件一定时,反应2A+B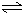 2C △H<0,A的最大转化率与温度关系曲线,下列叙述正确的是:( )
2C △H<0,A的最大转化率与温度关系曲线,下列叙述正确的是:( )

A.X或Y两点相应,V(正)>V(逆)
B.Z、N两点表示未达平衡状态,且都是V(正)>V(逆)
C.W点表示非平衡状态,V(正)>V(逆)
D.相应反应速率大小的点:W > Y > N
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省江淮十校高三8月联考化学试卷(解析版) 题型:填空题
(8分)利用化学原理可以对工厂排放的废水、废渣等进行有效检测。某工厂对制铬工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸液中金属离子主要是Cr3+,其次是Fe3+, Fe2+, Al3+, Ca2+, Mg2+)
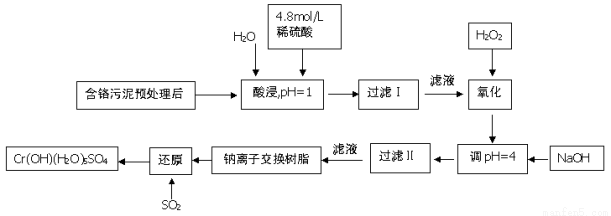
常温下部分阳离子的氢氧化物形成沉淀时溶液的pH见下表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Ca2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | 9.6 | 4.2 | 9.7 | — |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8.0 | 11.7 | 9.0(>9.0溶解) |
(1)酸浸时,为了提高浸取率可采取的措施是 (至少一条)
(2)调pH=4.0是为了除去 (填Fe3+, Al3+, Ca2+, Mg2+)
(3)钠离子交换树脂的原理为Mn+ + n NaR → MRn +nNa+,被交换的杂质离子是 (填Fe3+, Al3+, Ca2+, Mg2+)
(4)试配平下列氧化还原反应方程式:
Na2Cr2O7 + SO2 + H2O = Cr(OH)(H2O)5SO4 + Na2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com