
下列有关氧化还原反应的说法正确的是( )
A.浓盐酸在化学反应中既可以作氧化剂,又可以作还原剂
B.工业上常以SiO2为原料制取粗硅,这一过程中,硅元素被氧化
C.在任何条件下都不能发生反应:Cu + H2SO4====CuSO4+ H2↑
D.亚氯酸可发生分解反应:HClO2→ClO2↑+Cl2↑+H2O(未配平),1 mol HClO2分解时,转移电子的物质的量为1 mol
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。
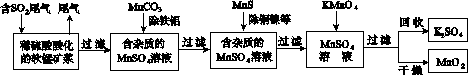
请回答下列问题:
(1)上述流程脱硫实现了____(选填下列字母编号)。
A.废弃物的综合利用
B.白色污染的减少
C.酸雨的减少
(2)用MnCO3能除去溶液中的Al3+和Fe3+,其原因是________________________________。
(3)已知:25 ℃、101 kPa时,
Mn(s)+O2(g)===MnO2(s) ΔH=-520 kJ/mol
S(s)+O2(g)===SO2(g) ΔH=-297 kJ/mol
Mn(s)+S(s)+2O2(g)===MnSO4(s)
ΔH=-1065 kJ/mol
SO2与MnO2反应生成无水MnSO4的热化方程式是____________________________________。
(4)MnO2可作超级电容器材料。用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是________________________________。
(5)MnO2是碱性锌锰电池的正极材料。碱性锌锰电池放电时,正极的电极反应式是________________。
(6)假设脱除的SO2只与软锰矿浆中的MnO2反应。按照图示流程,将a m3(标准状况)含SO2的体积分数为b%的尾气通入矿浆,若SO2的脱除率为89.6%,最终得到MnO2的质量为c kg,则除去铁、铝、铜、镍等杂质时,所引入的锰元素相当于MnO2________kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
含Cr2O72﹣的工业酸性废水会造成铬污染,排放前要进行如下处理:(Ⅰ)往工业废水中加入适量的NaCl搅拌均匀;(Ⅱ)以Fe做两电极进行电解,从而使溶液的pH不断升高,废水由酸性转化为碱性,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生:(Ⅲ)过滤回收沉淀,废水达到排放标准.
(1)在电解过程中,溶液pH不断升高的原因可能是
①电解时废水的体积不断减小 ②电解时H+在阴极被还原 ③作为阳极的Fe不断溶解 ④Cr2O72﹣转化为Cr3+时消耗了H+ ⑤NaCl在电解时转化成了NaOH
A.⑤B.②④C.②③④D.①②③④
(2)两极发生反应的电极反应式为
阳极: ;阴极: .
(3)写出Cr2O72﹣变成Cr3+的离子方程式 .
(4) (填“能”或“不能”)改用石墨电极进行电解.
查看答案和解析>>
科目:高中化学 来源: 题型:
关于0.1 mol·L-1Na2CO3溶液的叙述中错误的是 ( )
A.0.5 L该溶液中钠离子的物质的量浓度为0.2 mol·L-1
B.1 L该溶液中含有Na2CO3的质量为10.6 g
C.从1 L该溶液中取出100 mL,则取出溶液中Na2CO3的物质的量浓度为
0.01 mol·L-1
D.取该溶液10 mL,加水稀释至100 mL后,Na2CO3的物质的量浓度为0.01 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
将amL NO、bmL NO2、xmL O2混合于同一试管中,将试管倒插入水中,待气体与水充分反应后,试管内的气体全部消失,则x对a、b的函数关系式x=f(a,b)为 ( )

查看答案和解析>>
科目:高中化学 来源: 题型:
在一种酸性溶液中,可能存在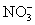 、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下的推测中不正确的是( )
、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下的推测中不正确的是( )
A.一定有碘离子 B.可能含铁离子
C.可能有氯离子 D.不含硝酸根离子
查看答案和解析>>
科目:高中化学 来源: 题型:
今有如下三个热化学方程式:
H2(g)+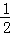 O2(g)═H2O(g)△H=a kJ•mol﹣1
O2(g)═H2O(g)△H=a kJ•mol﹣1
H2(g)+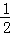 O2(g)═H2O(l)△H=b kJ•mol﹣1
O2(g)═H2O(l)△H=b kJ•mol﹣1
2H2(g)+O2(g)═2H2O(l)△H=c kJ•mol﹣1
关于它们的下列表述正确的是( )
|
| A. | 它们都是吸热反应 | B. | a、b和c均为正值 |
|
| C. | a=b | D. | 2b=c |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)原电池反应通常是放热反应,在理论上可设计成原电池的化学反应是 (填序号),理由是 该反应既 .
A.C(s)+H2O(g)═CO(g)+H2(g)△H>0
B.Ba(OH)2•8H2O(s)+2NH4Cl(s)═BaCl2(aq)+2NH3•H2O(l)+8H2O(l)△H>0
C.CaC2(s)+2H2O(l)═Ca(OH)2(s)+C2H2(g)△H<0
D.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H<0
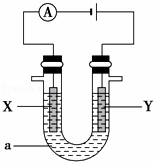
(2)电解原理在化学工业中有着广泛的应用.现将你设计的原电池通过导线与图中电解池相连,其中,a为电解液,X和Y是两块电极板,则:
①若X和Y均为惰性电极,a为饱和的NaCl溶液,则电解时,检验Y电极反应产物的方法是 .
②若X、Y分别为石墨和铁,a仍为饱和的NaCl溶液,则电解过程中生成的白色固体物质露置在空气中可观察到的现象为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com