
【题目】常温下,pH=1的乙酸溶液和pH=13的NaOH溶液,下列叙述中正确的是
A. 两种溶液等体积混合后,溶液呈碱性
B. 乙酸溶液中c(CH3COOH)大于NaOH溶液中c(Na+)
C. 分别稀释10倍,两溶液的pH之和大于14
D. 若两溶液混合后pH=7,则有c(Na+)=c(CH3COO-)+c(CH3COOH)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作、理象和结论均正确的是( )
选项 | 操作 | 现象 | 结论 |
A | 向某溶液中加入NaOH 溶液,并用湿润的红色石蕊试纸检验 | 试纸没有变蓝 | 原溶液中没有有NH4+ |
B | 向苏打和小苏打溶液中分别加入盐酸 | 均冒气泡 | 两者均能与盐酸反应 |
C | 向某溶液中滴加氯水后,再加KSCN溶液 | 溶液变红 | 原溶液中一定有Fe2+ |
D | 向某无色溶液中滴加BaCl2溶液 | 产生白色沉淀 | 该无色溶液中一定含有SO42- |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒酚是植物挥发油中的一种成分。关于胡椒酚的下列说法:

①该化合物属于芳香烃;
②分子中至少有7个碳原子处于同一平面;
③它的部分同分异构体能发生银镜反应;
④1 mol该化合物最多可与2 mol Br2发生反应。
其中正确的是( )
A. ②③ B. ①②④ C. ①③ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:_____与盐酸反应最剧烈,____与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl____S(填“>”或“<”),反应的离子方程式为_______。
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律。

(3)仪器A的名称为___________,干燥管D的作用为___________________。
(4)若要证明非金属性:Cl>I,C中为淀粉—碘化钾混合溶液,B中装有KMnO4固体,则A中试剂为___________,观察到C中溶液____________(填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用_________溶液吸收尾气。
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液。观察到C中溶液 ________(填现象),即可证明。但有的同学认为盐酸具有挥发性,HCl可进入C中干扰实验,应在两装置间添加装有 _________溶液的洗气瓶除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生活密切相关。回答下列问题:
(1)食品和药品关系人的生存和健康。
①市场上销售的食盐品种很多。下列食盐中,所添加的元素不属于人体必需微量元素的是__________(填序号字母,下同);
a.加钙盐 b.加碘盐 C.加锌盐
②纤维素被称为“第七营养素”。食物中含有的纤维素虽然不能为人体提供能量,但能促进肠道蠕动、吸附排除有害物质。在对有机物的分类中,纤维素属于__________;
a.蛋白质 b.脂肪 c.多糖
③下列药品中,服用后具有退烧效果的是_____________。
a.复方甘草麻黄碱片 b.复方阿司匹林片 c.复方氢氧化铝片
(2)材料是人类生存和发展的物质基础.合理使用材料可以改善我们的生活。
①在原子反应堆中广泛应用的钠钾合金在常温下呈液态.说明合金的熔点比其各成分金属的熔点___(选填“高”或“低”);
②炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会出现红褐色锈斑。我们将这种腐蚀方式称为_________________;
③人工合成的塑料有多种,其中聚丙烯是常见的食品级塑料,写出聚丙烯的结构简式__________。
(3)防治环境污染,改善生态环境已成为全球共识。
①下列物质中,进入大气会形成酸雨的是____________(填序号字母);
a.碳氧化物 b.硫氧化物 c.氮氧化物
②为治理“白色污染”,有人提出把塑料垃圾集中露天焚烧,这种处理方法的弊端是:__________(写出两项即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)Fe是人体不可缺少的微量元素,摄入含铁化合物可补充铁。硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定某补血剂中铁元素的含量。实验步骤如下:

请回答下列问题:
(1)步骤②中加入足量NaOH发生的主要反应的离子方程式为 ,
步骤③中反应的化学方程式为 。
(2)步骤④中一系列处理的操作步骤: 、洗涤、 、冷却、称量。
(3)若实验中需用98%的浓硫酸(密度为1.84g/mL)配制1 mol/L的稀硫酸480 mL。配制时用到的玻璃仪器除量筒、烧杯、胶头滴管、玻璃棒外还有 ,需用量筒量取该浓硫酸 mL。
(4)若实验无损耗,则每片补血剂含铁元素的质量 g(用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬元素及其化合物在生产、生活中具有广泛的用途。以某铬矿石(主要成分是Cr2O3,含FeO、SiO2等杂质)为原料生产Cr2O3的流程如下:
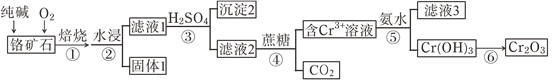
已知:主要反应是:2Cr2O3+4Na2CO3+3O2![]() 4Na2CrO4+4CO2
4Na2CrO4+4CO2
Cr2![]() +H2O
+H2O![]() 2Cr
2Cr![]() +2H+,Ksp[Cr(OH)3] =6.4×10-31,lg2 = 0.3
+2H+,Ksp[Cr(OH)3] =6.4×10-31,lg2 = 0.3
(1)Cr(OH)3和Al(OH)3性质类似,则Cr(OH)3与KOH反应的离子方程式为:_______;
(2)步骤⑤中为了使Cr3+完全沉淀[此时,c(Cr3+)≤10-5mol·L-1],pH至少调至_____;
(3)滤液3中的主要溶质是两种盐,化学式为_____、________;
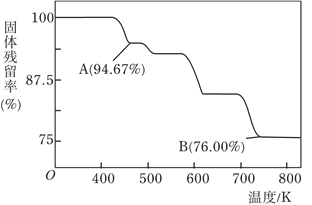
(4)CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示,则B点时剩余Cr的氧化物化学式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去括号内杂质所选试剂正确的是( )
A. Cu(CuO):稀硝酸B. FeCl3(AlCl3):氨水
C. Fe2O3(SiO2):NaOH溶液D. CO2(HCl):饱和Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制乙烯时,产生的气体能使溴水褪色,甲、乙同学用下列实验验证。
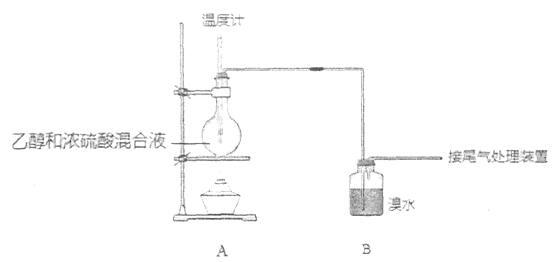
(气密性已检验,部分夹持装置略)。实验操作和现象为:
操作 | 现象 |
点燃酒精灯,加热至170℃ | I:A中烧瓶内液体渐渐变黑 II:B内气泡连续冒出,溶液逐渐褪色 |
…… | |
实验完毕,清洗烧瓶 | III:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(1)烧瓶内产生乙烯的化学方程式是________。
(2)溶液“渐渐变黑”,说明浓硫酸具有________性。
(3)分析使B中溶液褪色的物质,甲认为是C2H4,乙认为不能排除SO2的作用。
①根据甲的观点,使B中溶液褪色反应的化学方程式是________。
②乙根据现象III认为产生了SO2,在B中与SO2反应使溶液褪色的物质是________。
③为证实各自观点,甲、乙重新实验,设计与现象如下:
设计 | 现象 | |
甲 | 在A、B间增加一个装有某种试剂的洗气瓶 | 溴水褪色 |
乙 | 与A连接的装置如下:
| D中溶液由红棕色变为浅红棕色时,E中溶液褪色 |
a. 根据甲的设计,洗气瓶中盛放的试剂是________。
b. 根据乙的设计,C中盛放的试剂是________。
c. 能证明确实是SO2使E中溶液褪色的实验是________。
d. 乙为进一步验证其观点,取少量D中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是________。
(4)上述实验得到的结论是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com