

| A.虚线框内接灵敏电流计,该装置可将化学能转化为电能 |
B.虚线框中接直流电源,可能发生反应:Cu + H2SO4  CuSO4 + H2↑ CuSO4 + H2↑ |
C.虚线框内接直流电源,可能发生反应:Zn + H2SO4  ZnSO4 + H2↑ ZnSO4 + H2↑ |
| D.生成2.24 LH2时,一定转移0.2 mol电子 |
科目:高中化学 来源:不详 题型:单选题
| A.在101kpa下,1mol物质完全燃烧的反应热叫做该物质的热值。 |
| B.盐桥通常用含CuCl2的饱和溶液的琼脂的离子移动来平衡溶液中的电荷。 |
| C.在交流电的作用下,在两电极分别发生氧化反应和还原反应的过程叫电解。 |
| D.金属材料电镀时,通常把待镀金属制品放在阴极。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
| B.工业上用石灰乳对煤燃烧后形成的烟气进行脱硫,最终能制得石膏 |
| C.现代常用红外光谱仪、核磁共振仪研究有机化合物的结构 |
| D.MgO、Al2O3的熔点很高,工业上用于制作耐高温材料,也用于冶炼镁、铝金属 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
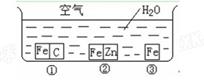
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在金属表面喷漆 |
| B.在金属中加入一些铬或镍制成合金 |
| C.在轮船的壳体水线以下部分装上锌块 |
D.使金属表面生成致密稳定的氧化物保护 膜 膜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com