
【题目】下列关于溶液的说法正确的是
A. 溶液都是均一、稳定的纯净物
B. 饱和溶液的浓度一定大于不饱和溶液的浓度
C. 钠与氧气反应只能生成氧化钠
D. 实验室制取氯气的原料可选用浓盐酸和二氧化锰
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源: 题型:
【题目】《茶疏》中对泡茶过程有如下记载:“治壶、投茶、出浴、淋壶、烫杯、酾茶、品茶……”。文中未涉及的操作方法是
A. 溶解 B. 萃取 C. 过滤 D. 蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C5H7Cl的有机物,其结构不可能是( )
A.只含有1个双键的直链有机物
B.含2个双键的直链有机物
C.含1个双键的环状有机物
D.含一个三键的直链有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应最终没有固体析出的是
A. 向氯化钡溶液中通入少量CO2
B. 向饱和氢氧化钠溶液中加入钠单质
C. 向饱和碳酸钠溶液中通入过量CO2
D. 向NaHCO3溶液中加入过量澄清石灰水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 在含A13+总数为NA的A1C13溶液中,C1-总数为3NA
B. 标准状况下,5.6L CO2中含有的共用电子对数为0.5NA
C. Na2O2与足量的CO2反应生成0.1mol O2,转移的电子数为0.2NA
D. 常温下,56g铁片投入足量浓H2SO4中,充分反应,生成NA个SO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中,发生3A(g)+B(g)2C(g)的反应,若最初加入A和B都是4mol,A的平均反应速率为0.12molL﹣1s﹣1,则10s后容器中B的物质的量是( )
A. 1.6 mol B. 2.8 mol C. 3.2 mol D. 3.6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液的酸碱性可用酸度(AG)表示AG=lg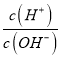 。室温下,某化学兴趣小组的同学用 0.01 mol·L-1的氢氧化钠溶液滴定20.00 mL 0.01 mol·L-1醋酸,滴定结果如下图所示,下列有关叙述中正确的是
。室温下,某化学兴趣小组的同学用 0.01 mol·L-1的氢氧化钠溶液滴定20.00 mL 0.01 mol·L-1醋酸,滴定结果如下图所示,下列有关叙述中正确的是
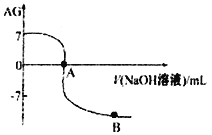
A. 水的电离程度A点小于B点
B. A点时加入的氢氧化钠溶液的体积恰好为20.00 mL
C. 室温0.01 mol·L-1醋酸溶液的电离平衡常数Ka=l0-5
D. 若B点时所加NaOH溶液的体积为40.00 mL,此时溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中常见非金属元素形成的化合物与新能源和新环境问题密切相关。
(1)我国于2016年10月17日由长征号FY11运载火箭发射神舟十号飞船,其推力能量主要是压缩成液体燃料(CH3)2N-NH2和氧化剂N2O4,该燃料组燃烧后产生巨大能量,释放产物为无毒无害的气体。298K时,10g燃料完全燃烧释放的能量为425kJ,请写出该反应的热化学方程式
_____________。
(2)二氧化硫、氮氧化物以及可吸入颗粒物(PM2.5 等)这三项是雾霾主要组成。其中炭还原法处理氮氧化物是一种方法。T℃时反应C(s)+2NO(g)![]() N2(g) + CO2(g),反应始终从反应物投料开始,测定各时间点的物质浓度图像如下:
N2(g) + CO2(g),反应始终从反应物投料开始,测定各时间点的物质浓度图像如下:

① 第一次平衡前,CO2的平均反应速率v (CO2)=____________;
② 若反应在T℃进行,只改变起始反应物投料,某时刻测得C(NO)=4 mol/L, C(N2) =4mol/L,则此时V(正)_____V(逆)(填“>”、“<”或“=”) ;
③ 根据图像判断,40min时改变的条件可能是__________;
A.恒压条件下通入NO; B.升高温度; C.(恒容条件)通入NO; D.压缩体积;
E.恒压时加入活性炭; F.使用新型催化剂。
(3)新能源应用探索中,可以用下图装置于净化处理厕所排放废水中的尿素(H2NCONH2),同时产生电能。请写出负极电极反应式:_____________;

(4)工业上使用氨碱吸收SO2,然后使之转化成NH4HSO4,可作分析试剂使用,现用0.1mol/LKOH来滴定100mL0.1mol/L NH4HSO4,反应过程的滴定曲线如下图:
已知:常温时NH3·H2O的电离常数K=1.8×10-5,忽略溶液混合后体积变化,请根据图中给出的5个点的字母回答相关问题。

①滴定过程中以上5个点中,_________点水电离程度最小;
②滴定过程中Z点溶液中各离子浓度由大到小的排列顺序是_________;
③滴定过程中M点的pH大约是(填整数)___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com